เนื้อหาดูได้ที่: English (อังกฤษ) Indonesia (อินโดนีเซีย) Tiếng Việt (เวียดนาม)
โรคนิวคาสเซิล: การรู้จักไวรัสให้ดีขึ้น เพื่อตัดสินใจควบคุมได้ดีที่สุด ตอนที่ 1
โรคนิวคาสเซิล (ND) ถือเป็นหนึ่งในโรคติดเชื้อที่สำคัญที่สุดในสัตว์ปีก เนื่องจากไวรัสสายพันธุ์เวโลเจนิกสามารถทำให้เกิดการระบาดที่มีอัตราการเจ็บป่วยและเสียชีวิตสูง การจำกัดการค้าระหว่างประเทศ
- ทำให้เกิดผลสำคัญ การสูญเสียทางเศรษฐกิจต่ออุตสาหกรรมสัตว์ปีกนี่คือสาเหตุที่โรคนี้รวมอยู่ในรายชื่อโรคที่ต้องแจ้งต่อองค์กรสุขภาพสัตว์โลก (มิลเลอร์และโคช, 2020)
- โรคนิวคาสเซิลป้องกันได้ด้วยการป้องกันทางชีวภาพและการฉีดวัคซีน แม้ว่าจะมีการนำวัคซีนที่มีชีวิตและวัคซีนชนิดเชื้อตายที่มีประสิทธิผลหลายประเภทมาใช้ แต่โรคนิวคาสเซิลยังคงเป็นปัญหาในหลายประเทศทั่วโลก
ตัวแทนแห่งเหตุ
ฐานข้อมูลคณะกรรมการระหว่างประเทศว่าด้วยอนุกรมวิธานไวรัสจัดประเภทไวรัสเป็นวงศ์ Paramyxoviridaeซึ่งเป็นวงศ์ย่อย
Avulavirinae โดยวงศ์หลังนี้กระจายอยู่ในสามสกุล:
- ออร์โธวูลาไวรัส
- เมตาวูลาไวรัส
- พาราวูลาไวรัส
พารามิกโซไวรัสของไก่ ถูกแยกออกมาจากสายพันธุ์ไก่ที่แตกต่างกัน และจำแนกออกเป็น 21 ซีโรไทป์ โดยการทดสอบทางเซรุ่มวิทยาและการวิเคราะห์เชิง
วิวัฒนาการ (WOAH, 2021)
- โรคนิวคาสเซิลเกิดจากเชื้อไวรัสAvian Paramyxovirus ชนิด 1(APMV-1) สายพันธุ์ที่ก่อโรค และเชื้อไวรัส Avian Orthoavulavirusชนิด 1 (OAV-1) สายพันธุ์ที่ก่อโรค
ไวรัสโรคนิวคาสเซิล (NDV) มี จีโนมอาร์เอ็นเอแบบสายเดี่ยว ไม่แบ่งส่วน และมีความรู้สึกเชิงลบ โดยมีนิวคลีโอไทด์จำนวน15,186 ตัว (Alexander, 2003)
ไวรัสมีชั้นไขมันสองชั้น เยื่อหุ้มที่ได้มาจากเยื่อหุ้มพลาสมา ของเซลล์โฮสต์(มาสต์ เดอมีเอสเทียร์, 2009)
จีโนมของไวรัสประกอบด้วยยีน 6 ยีนในลำดับ 3′-NP-PMF-HN-L-5′ ซึ่งเข้ารหัสโปรตีนของไวรัส 7 ตัว:
- นิวคลีโอโปรตีน (NP),
- ฟอสโฟโปรตีน (P),
- โปรตีนเมทริกซ์ (M),
- โปรตีนฟิวชั่น (F),
- เฮแมกกลูตินิน-นิวรามินิเดส (HN)
- RNA โพลิเมอเรส เรียกว่า โพลิเมอเรสขนาดใหญ่ (L)
การตัดต่อ RNA ของโปรตีน P ทำให้เกิด โปรตีนเพิ่มเติมคือโปรตีน V ซึ่งมีฤทธิ์ต้านอินเตอร์เฟอรอน ซึ่งช่วยให้ไวรัสสามารถต่อต้านการตอบสนองของเซลล์โฮสต์โดยกำเนิดได้ (มิลเลอร์และโคช,2020) (รูปที่ 1)
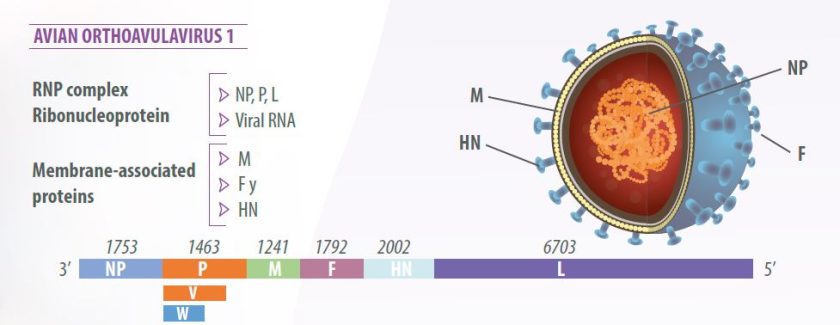
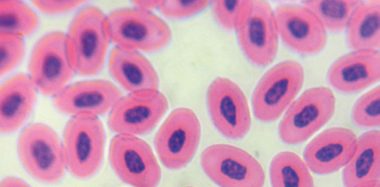
คุณสมบัติทางชีววิทยาหลักของไวรัสคือการจับกลุ่มเม็ดเลือดแดงของไก่สัตว์สะเทินน้ำสะเทินบก และสัตว์เลื้อยคลาน เนื่องจาก การกระทำของโปรตีนHN บนตัวรับกรดซาลิกที่อยู่บนพื้นผิวของเม็ดเลือดแดง
การเกาะกลุ่มของไวรัส (HA) ช่วยให้สามารถระบุการมีอยู่ของไวรัสในวัฒนธรรมไวรัสและของเหลวในอัลลันโทอิกได้ ของตัวอ่อนไก่ (มิลเลอร์และโคช, 2020), และการวัดปริมาณแอนติบอดีในซีรั่มนกด้วยการทดสอบการยับยั้งการเกาะกลุ่มของเม็ดเลือด (HAI)
ผลของการทำลายเซลล์มะเร็ง ของไวรัส NDV บางสายพันธุ์ต่อเซลล์เนื้องอกในมนุษย์และการนำมาใช้ในการรักษามะเร็งในมนุษย์ได้รับการศึกษามาเป็นเวลานานแล้ว
- ต้านอินเตอร์เฟอรอนชนิด I ของโปรตีน V
การจำลองแบบเลือกที่ไวรัสมีในเซลล์เนื้องอกเกิดจากข้อบกพร่องของเซลล์เหล่านี้ในการกระตุ้นเส้นทางการส่งสัญญาณ IFN ชนิด I และเส้นทางอะพอพโทซิส เป็นต้น (ชิร์มาเคอร์,2017)
การจำลองไวรัส
NDV จำลองแบบในไซโตพลาซึมของเซลล์ เฮแมกกลูตินิน HN) จดจำตัวรับเซลล์โดยกระตุ้นโปรตีน F เพื่อหลอมรวมเยื่อหุ้มเซลล์และไวรัส ทำให้ไวรัสเข้าสู่ไซโทพลาซึมได้โดยการเอนโดไซโทซิส (Bergfeld,2017; Miller and Koch, 2020) ยีนทั้งหมดเข้ารหัสโปรตีนหลักตัวเดียวอย่างไรก็ตาม ยีน P mRNA ผลลัพธ์ในการก่อตัวของโปรตีนที่ไม่ใช่โครงสร้างสองชนิดคือโปรตีน V และโปรตีน W (Vilela et al., 2022)
- คอมเพล็กซ์ไรโบนิวคลีโอโปรตีน (RPN)ประกอบด้วยจีโนม RNA ที่ห่อหุ้มด้วยนิวคลีโอโปรตีน (NP) ซึ่งเกี่ยวข้องกับคอมเพล็กซ์โพลีเมอเรสที่ประกอบด้วยฟอสโฟโปรตีน (P) และโปรตีนขนาดใหญ่ (L)
- หลังจากที่นิวคลีโอแคปไซด์ของไวรัสเข้าสู่ไซโทพลาซึมแล้ว มันจะแยกตัวออกจากโปรตีน M และถูกปล่อยออกมาเพื่อเริ่มต้นการสังเคราะห์ mRNA ที่จำเป็นสำหรับการแปลโปรตีนของไวรัส
- โปรตีน P ทำหน้าที่เป็นตัวกลางในการจับกันของคอมเพล็กซ์โพลีเมอเรสกับนิวคลีโอแคปไซด์ และโปรตีน Lทำหน้าที่เร่งปฏิกิริยาของโพลีเมอเรส (Dortmans et al.,2011; Cox และPlemper, 2017)
- ยีนทั้งหมดเข้ารหัสโปรตีนหลักตัวเดียวอย่างไรก็ตาม ยีน P mRNA ผลลัพธ์ในการก่อตัวของโปรตีนที่ไม่ใช่โครงสร้างสองชนิดคือโปรตีน V และโปรตีน W (Vilela et al., 2022)
1. หลังจากที่ mRNA ถูกแปลเป็นโปรตีนของไวรัสแล้ว จีโนมที่มีขั้วลบจะทำการจำลองตัวเอง โดยผลิต RNA ต้านจีโนม ซึ่งทำหน้าที่เป็นแม่แบบสำหรับการสังเคราะห์จีโนม RNA ขนาดเต็ม (Miller และ Koch, 2020; Dortmans และคณะ, 2011)
2. โปรตีน HN ที่ถูกสังเคราะห์ภายในเซลล์จะถูกลำเลียงไปยังเยื่อหุ้มเซลล์ผ่านการแทรกตัว จากนั้นนิวคลีโอแคปซิดและ RNA ของไวรัสจะจัดเรียงตัวเข้ากับบริเวณที่มีการเปลี่ยนแปลงของเยื่อหุ้มเซลล์ ซึ่งเป็นบริเวณที่มีไกลโคโปรตีนของไวรัส (Miller และ Koch, 2020)
- โปรตีนเมทริกซ์ M ทำหน้าที่จัดระเบียบการประกอบตัวของอนุภาคไวรัส โดยมีปฏิสัมพันธ์กับโปรตีน N ของคอมเพล็กซ์ RNP และคอมเพล็กซ์ไกลโคโปรตีนที่ฝังอยู่ในเยื่อหุ้มเซลล์ (Cox และ Plemper, 2017)
3. อนุภาคไวรัสใหม่จะถูกปล่อยออกโดยการบัดดิ้ง (budding) จากผิวเซลล์ โดยดึงพาไลโปโปรตีนที่เป็นเยื่อหุ้มของเซลล์ออกมาด้วย (Miller และ Koch, 2020; Cox และ Plemper, 2017)
4. นิวรามินิเดสของโปรตีน HN มีบทบาทในการปล่อยไวรัสออกจากเซลล์ โดยการกำจัดตัวรับของเซลล์ (Bergfeld, 2017)
ความก่อโรคจากไวรัส
ตามอาการทางคลินิกที่เกิดขึ้นในไก่ที่ติดเชื้อสายพันธุ์ NDV แบ่งได้ดังนี้:
- สายพันธุ์ viscerotropic velogenic(vvVEN) และสายพันธุ์ mesogenic (ทั้งสองชนิดก่อให้เกิดโรค Newcastle) และ
- สายพันธุ์ที่ก่อให้เกิดโรคเลนโตและโรคลำไส้หรือโรคที่ไม่ก่อโรค (ใช้เป็นวัคซีน)
องค์กรสุขภาพสัตว์โลก (WOAH) ได้กำหนดว่า สายพันธุ์ของ APMV-1 จะก่อโรคได้เมื่อมีลักษณะดังต่อไปนี้:
- ดัชนีความก่อโรคภายในกะโหลกศีรษะ (IPIC) เท่ากับหรือมากกว่า0.7 (โดยคำนึงถึงค่าต่ำสุดและค่าสูงสุดจาก 0 ถึง 2) หรือ
- ไซต์การแยกโปรตีน F ประกอบด้วยกรดอะมิโนเบสหลายชนิดและมีฟีนิลอะลานีนอยู่ที่ตำแหน่ง 117(WOAH, 2021)
เอฟ-ไกลโคโปรตีนเป็นกุญแจสำคัญต่อความรุนแรงของไวรัสและการเกิดโรค เนื่องจากการเข้าสู่เซลล์ขึ้นอยู่กับการหลอมรวมของไวรัสและเยื่อหุ้มเซลล์หลังจากการแยกโปรตีน F0 ออกเป็น F1และ F2 โดยโปรตีเอสของโฮสต์(Miller และ Koch, 2020)
ความแตกต่างระหว่างไวรัสก่อโรคกับไวรัสไม่ก่อโรคคือ:
- ไวรัสที่มีลำดับกรดอะมิโนเบสเดียวที่ไซต์การแยก F0 เป็นไวรัสที่ไม่มีเชื้อเพราะว่า: สารตั้งต้นนี้จะอ่อนไหวต่อเอนไซม์ที่ขับออกมาจากเยื่อเมือก เช่น ทริปซินเท่านั้น จึงทำให้เกิดการติดเชื้อเฉพาะที่
ในทางกลับกัน ไวรัสที่มีลำดับไดบาซิกจะก่อโรค เนื่องจากเป็น:
- ไวต่อเอนไซม์ภายในเซลล์ที่มีอยู่ทั่วไป ซึ่งทำให้ไวรัสแพร่กระจายและทำให้เกิดการติดเชื้อในระบบและถึงแก่ชีวิตได้ (Czeglédiet al., 2006; Miller และ Koch, 2020)
ดัชนีการก่อโรคภายในกะโหลกศีรษะ
ดัชนีความก่อโรคภายในกะโหลกศีรษะ(IPIC) เป็นวิธีที่ดีที่สุดในการตรวจสอบความก่อโรคของไวรัส เนื่องจากไม่เพียงแต่กำหนดความก่อโรคของสายพันธุ์เท่านั้น แต่ยังวัดเป็นค่าต่างๆ ได้ด้วย
ไวรัสจะถือว่ามีความเป็นโรค (pathogenic) เมื่อมีค่าดัชนีความรุนแรงในสมอง (IPIC) เท่ากับหรือมากกว่า 0.7 (WOAH, 2021) โดยความรุนแรงของไวรัสจะแตกต่างกันอย่างมากในแต่ละสายพันธุ์ ตารางที่ 1 แสดงสรุปค่าดัชนีความรุนแรงของไวรัสในแต่ละชนิด (pathotype) ที่ได้จากการทดสอบในรูปแบบต่าง ๆ (Alexander, 1989 และ 1998)
- ของเหลวอัลแลนทอยิกที่ยืนยันผลบวกในการตรวจหา Hemagglutinin (HA) โดยมีค่าไตเตอร์การจับตัวของเม็ดเลือดแดงมากกว่า 1:16 จะถูกทำให้เจือจางในอัตราส่วน 1:10 ด้วยสารละลายเกลือ จากนั้นฉีดเข้าทางสมองของลูกไก่ SPF อายุ 1 วัน จำนวน 10 ตัว ในปริมาณ 0.05 มิลลิลิตร
- ลูกไก่จะถูกตรวจสอบอาการทุกวันเป็นระยะเวลา 8 วัน โดยกำหนดคะแนนรายวันดังนี้:0 หากมีอาการปกติ, 1 หากมีอาการป่วย 2 หากตาย
- ลูกไก่ที่ตายจะได้รับคะแนน 2 ทุกวันถัดไปจนถึงวันที่ 8
- ค่าดัชนี IPIC คำนวณจากค่าเฉลี่ยของคะแนนรายวันต่อลูกไก่หนึ่งตัวในระยะเวลา 8 วัน โดยไวรัสที่มีความรุนแรงสูงสุดจะมีค่าดัชนีใกล้ 2.0 ขณะที่ไวรัสชนิดที่มีความรุนแรงต่ำ (lentogenic virus) จะมีค่าดัชนีใกล้ 0.0
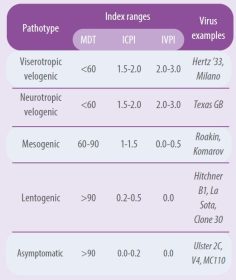
ไวรัส APMV-1 ทุกไอโซเลตถือว่าอยู่ในเซอโรไทป์เดียวกัน อย่างไรก็ตาม มีรายงานการพบความแตกต่างทางแอนติเจนในบางไอโซเลตจากการทดสอบด้วยวิธีต่าง ๆ และถึงแม้จะไม่มีความแตกต่างทางแอนติเจนระหว่างสายพันธุ์ การวิเคราะห์ทางพันธุกรรมได้กลายเป็นวิธีหลักในการจำแนกลักษณะของไวรัส และได้เข้ามาแทนที่การใช้แอนติบอดีจำเพาะ (monoclonal antibodies, mAbs) ในการจำแนกชนิดของไวรัส NDV แล้ว
การกำหนดจีโนไทป์ของไวรัส
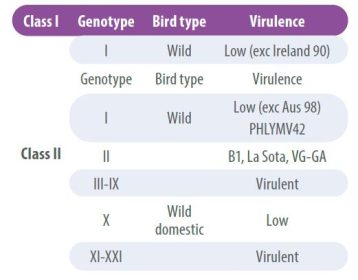
ไวรัส NDV มีอัตราการรวมตัวใหม่ต่ำอย่างไรก็ตาม เมื่อเวลาผ่านไป ได้มีการตรวจพบความแตกต่างของแอนติเจนบางประการ ซึ่งนำไปสู่การจำแนกสายพันธุ์เป็นวงศ์ตระกูลหรือจีโนไทป์ ดังนั้น สายพันธุ์ต่างๆ จะถูกแบ่งเป็น 2 กลุ่มหลัก คือ ไวรัสคลาส I และไวรัสคลาส II
- ไวรัสคลาส I มีความก่อโรคต่ำ และพบได้ในนกป่า
- ในทางกลับกัน คลาส II จะถูกแบ่งออกเป็นจีโนไทป์หลายประเภท และอาจเป็นแบบไม่ก่อโรคหรือเป็นเชื้อก่อโรคร้ายแรงก็ได้(ตารางที่ 2)
ลักษณะเฉพาะของจีโนไทป์ NDV ทำได้โดยการเรียงลำดับยีน F ทั้งหมด ซึ่งช่วยให้สามารถกำหนดความรุนแรงของโรค
ได้ด้วย
- เพื่อระบุจีโนไทป์ใหม่ จะใช้ระบบที่อิงตามระยะทางวิวัฒนาการเฉลี่ย 10% ระหว่างกลุ่มพันธุกรรม (ดิมิทรอฟ KM และคณะ2016; ดิมิทรอฟ KM และคณะ 2019)
การพัฒนาการจัดลำดับรุ่นถัดไป (NGS)กลายมาเป็นเครื่องมือสำหรับการวิจัยและการระบุลักษณะทางพันธุกรรมของเชื้อก่อโรค
- อย่างไรก็ตาม วิธีนี้เหมาะอย่างยิ่งสำหรับไวรัส RNA ที่กลายพันธุ์อย่างรวดเร็ว ซึ่งจำเป็นต้องมีการวิเคราะห์ด้านวิวัฒนาการด้วย (บัตต์และคณะ, 2019)
การจำแนกประเภทจีโนไทป์ปัจจุบันประกอบด้วยจีโนไทป์ใหม่ 3 แบบ (XIX, XX และ XXI)ทำให้มีจีโนไทป์ไวรัสทั้งหมด 21 แบบในไวรัสคลาส II ( ดิมิโทรฟและคณะ (2019).
ความต้านทานต่อสารทางกายภาพและเคมี
เนื่องจากเป็น ไวรัสที่มีเยื่อหุ้ม ความสามารถในการดำรงชีวิตของParamyxovirus ในนก จึงถูกทำลายได้ง่าย ด้วยปัจจัยทางกายภาพและเคมี เช่น:
- ความร้อน,
- แสงอุลตราไวโอเลต,
- กระบวนการออกซิเดชัน
- ค่า pH และ
- การบำบัดด้วยสารฆ่าเชื้อส่วนใหญ่
อย่างไรก็ตามการตีพิมพ์เกี่ยวกับไวรัส เวลาเอาตัวรอด ภายนอกโฮสต์แสดงความแตกต่างที่เกิดจากอุณหภูมิความชื้น และสภาพแวดล้อมที่วิเคราะห์ไวรัส (คินเดและคณะ, 2004)
🔒 เนื้อหาเฉพาะสำหรับผู้ใช้ที่ลงทะเบียน.
ลงทะเบียนฟรีเพื่อเข้าถึงโพสต์นี้และเนื้อหาเฉพาะทางอื่น ๆ อีกมากมาย ใช้เวลาเพียงหนึ่งนาทีและคุณจะสามารถเข้าถึงได้ทันที
เข้าสู่ระบบลงทะเบียนได้ที่ aviNews
ลงทะเบียน














