Nội dung có ở: English Indonesia (Indonesian) ไทย (Thai)
Bệnh Newcastle: Hiểu rõ virus để đưa ra quyết định kiểm soát tốt nhất. Phần I
Newcastle (ND) được coi là một trong những bệnh truyền nhiễm quan trọng nhất ở gia cầm vì các chủng virus độc lực cao có thể gây ra các đợt bùng phát với tỷ lệ mắc bệnh và tử vong cao, đồng thời gây hạn chế thương mại quốc tế.
- Điều này gây ra tổn thất kinh tế đáng kể cho ngành chăn nuôi gia cầm. Đó là lý do bệnh này được liệt kê vào danh sách các bệnh bắt buộc báo cáo cho Tổ chức Thú y Thế giới (Miller và Koch, 2020).
- Bệnh Newcastle được phòng ngừa bằng các biện pháp an toàn sinh học và tiêm phòng; mặc dù đã áp dụng nhiều loại vắc-xin sống và bất hoạt hiệu quả, bệnh ND vẫn tiếp tục là vấn đề ở nhiều quốc gia trên thế giới.
YẾU TỐ GÂY BỆNH
Cơ sở dữ liệu của Ủy ban Quốc tế về Phân loại Virus phân loại virus này thuộc họ Paramyxoviridae, phân họ Avulavirinae, trong đó phân họ này được chia thành ba chi:
- Orthoavulavirus.
- Metaavulavirus.
- Paravulavirus.
Các virus paramyxovirus gia cầm đã được phân lập từ nhiều loài gia cầm khác nhau và được phân loại thành 21 kiểu huyết thanh thông qua các xét nghiệm huyết thanh học và phân tích phát sinh chủng loài (WOAH, 2021).
- Bệnh Newcastle do các chủng độc lực của Avian Paramyxovirus type 1 (APMV-1), thuộc loài Avian Orthoavulavirus type 1 (OAV-1) gây ra.
Virus gây bệnh Newcastle (NDV) có genome có RNA đơn sợi, không phân đoạn, mang tính âm, với độ dài 15.186 nucleotit ( Alexander, 2003).
Virion có một lớp màng lipid kép được lấy từ màng plasma của tế bào chủ (Mast và Demeestere, 2009).
Genome của virus bao gồm sáu gen theo thứ tự 3’-NP-P-M-F-HN-L-5’, mã hóa cho bảy loại protein virus:
- Nucleoprotein (NP),
- Phosphoprotein (P),
- Protein cấu trúc màng (Matrix protein, M),
- Protein hòa màng (Fusion protein, F),
- Hemagglutinin-neuraminidase (HN) và
- RNA polymerase, gọi là large polymerase (L).
Sửa đổi RNA của protein P tạo ra một protein bổ sung là protein V, có hoạt tính chống interferon, cho phép virus chống lại phản ứng tự nhiên của tế bào chủ (Miller và Koch, 2020) (Hình 1).
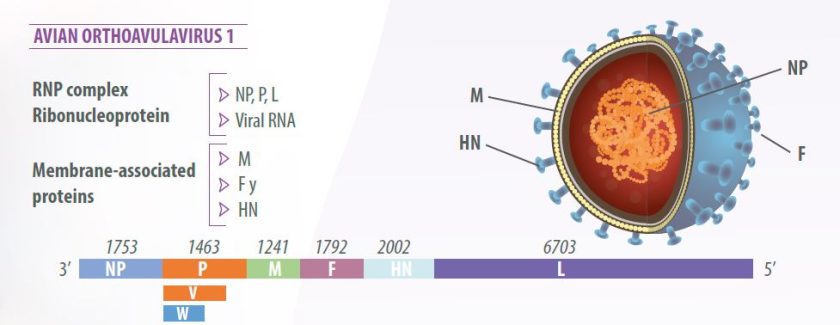
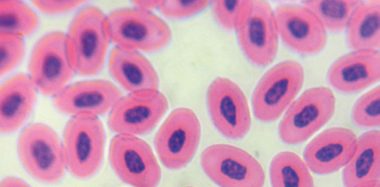
Đặc tính sinh học chính của virus là khả năng ngưng kết hồng cầu của các loài gia cầm, lưỡng cư và bò sát, do tác động của protein HN lên các thụ thể axit sialic trên bề mặt hồng cầu.
Hiện tượng ngưng kết hồng cầu (HA) cho phép xác định sự hiện diện của virus trong các môi trường nuôi cấy virus và trong dịch màng niệu của phôi gà (Miller và Koch, 2020), đồng thời định lượng kháng thể trong huyết thanh của gia cầm thông qua xét nghiệm ức chế ngưng kết hồng cầu (HAI).
Tác dụng tiêu diệt tế bào ung thư (oncolytic) của một số chủng NDV lên các tế bào ung thư người và khả năng sử dụng chúng làm phương pháp điều trị ung thư ở người đã được nghiên cứu trong một thời gian.
- Hiệu ứng này liên quan đến hoạt tính chống interferon type I của protein V.
Khả năng nhân lên có chọn lọc của virus trong tế bào khối u là do các khiếm khuyết trong các tế bào này về khả năng kích hoạt các con đường tín hiệu interferon type I và các con đường gây chết tế bào theo chương trình (apoptosis), cùng các cơ chế khác (Schirrmacher, 2017).
QUÁ TRÌNH NHÂN LÊN CỦA VIRUS
NDV (virus gây bệnh Newcastle) nhân lên trong bào tương của tế bào. Protein hemagglutinin (HN) nhận diện thụ thể của tế bào, sau đó kích hoạt protein F để hợp nhất màng virus và màng tế bào, cho phép virus xâm nhập vào bào tương thông qua quá trình nhập bào (endocytosis) (Bergfeld, 2017; Miller và Koch, 2020).
- Phức hợp ribonucleoprotein (RNP) chứa genome RNA được bao bọc bởi nucleoprotein (NP), kết hợp với phức hợp polymerase gồm phosphoprotein (P) và protein lớn (L);
- Sau khi nucleocapsid của virus xâm nhập vào bào tương, nó tách khỏi protein M và được giải phóng để bắt đầu quá trình tổng hợp mRNA cần thiết cho việc dịch mã các protein virus.
- Sửa đổi RNA của protein P tạo ra một protein bổ sung là protein V, có hoạt tính chống interferon, cho phép virus chống lại phản ứng tự nhiên của tế bào chủ (Miller và Koch, 2020) (Hình 1).
- Tất cả các gen đều mã hóa cho một protein chính, tuy nhiên, MRNA của gen P có thể tạo ra hai protein không cấu trúc là protein V và protein W(Vilela et al., 2022).
1. After the mRNA is translated into viral proteins, the negative polarity genome replicates, producing an anti-genomic RNA that serves as a template for the synthesis of a full-length genomic RNA (Miller and Koch, 2020; Dortmans et al., 2011). Sau khi mRNA được dịch mã thành các protein virus, bộ gen có cực âm sẽ nhân lên, tạo ra RNA kháng gen đóng vai trò làm khuôn mẫu cho quá trình tổng hợp RNA bộ gen đầy đủ (Miller và Koch, 2020; Dortmans và cộng sự, 2011).
2. Các protein HN được tổng hợp trong tế bào sẽ được vận chuyển đến màng tế bào thông qua quá trình chèn vào màng, sau đó nucleocapsid và RNA của virus sẽ sắp xếp thẳng hàng với các vùng màng tế bào lân cận đã được biến đổi, những vùng này chứa các glycoprotein của virus (Miller và Koch, 2020).
- Protein ma trận M tổ chức quá trình lắp ráp các hạt virus thông qua sự tương tác với các protein N của phức hợp RNP và các phức hợp glycoprotein tích hợp trong màng (Cox và Plemper, 2017).
3. Các hạt virus mới thoát ra ngoài bằng cách nảy chồi từ bề mặt tế bào, kéo theo lớp vỏ lipoprotein của tế bào (Miller và Koch, 2020; Cox và Plemper, 2017).
4. Neuraminidase của protein HN cho phép virus được giải phóng khỏi tế bào bằng cách loại bỏ thụ thể của tế bào (Bergfeld, 2017).
ĐỘC LỰC CỦA VIRUS
Dựa trên các dấu hiệu lâm sàng mà chúng gây ra ở gia cầm nhiễm bệnh, các chủng NDV được phân loại như sau:
- Chủng velogenic viscerotropic (vvVEN) và chủng mesogenic (cả hai đều gây bệnh Newcastle), và
- Chủng lentogenic và chủng ở đường ruột hoặc không gây bệnh (apathogenic) (được sử dụng làm vắc xin).
Tổ chức Thú y Thế giới (WOAH) xác định rằng một chủng APMV-1 được coi là độc lực khi nó có:
- Chỉ số gây bệnh nội sọ (Intracranial Pathogenicity Index – IPIC) bằng hoặc lớn hơn 0,7 (giá trị tối thiểu và tối đa từ 0 đến 2); hoặc,
- Vị trí cắt của protein F có nhiều axit amin mang điện dương (basic amino acids) và có phenylalanine ở vị trí 117 (WOAH, 2021).
Glycoprotein F là yếu tố then chốt quyết định độc lực và cơ chế gây bệnh của virus, vì việc xâm nhập vào tế bào phụ thuộc vào sự hợp nhất giữa màng virus và màng tế bào sau khi protein F0 bị cắt thành F1 và F2 bởi các protease của vật chủ ( Miller và Koch, 2020).
Sự khác biệt giữa virus độc lực và không độc lực là: Các virus có trình tự amino acid đơn cơ bản (monobasic) tại vị trí cắt của F0 được coi là không gây bệnh (apathogenic) vì:
- Cơ chất này chỉ dễ bị phân giải bởi các enzyme có trong màng nhầy, như trypsin, do đó chỉ gây ra nhiễm trùng cục bộ.
Ngược lại, virus có trình tự dibasic là virus có độc lực vì chúng:
- Dễ bị phân cắt bởi các enzyme nội bào phổ biến, cho phép virus lan rộng và gây nhiễm trùng toàn thân, nguy hiểm đến tính mạng (Czeglédi et al., 2006; Miller và Koch, 2020).
CHỈ SỐ BỆNH LÝ NỘI SỌ (INTRACRANIAL PATHOGENICITY INDEX)
Chỉ số bệnh lý nội sọ (IPIC) là phương pháp tốt nhất để xác định mức độ độc lực của virus, vì nó không chỉ cho biết chủng virus có độc lực hay không mà còn định lượng bằng giá trị cụ thể.
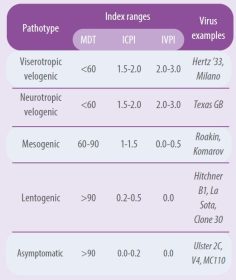
Một loại virus được coi là có độc lực khi nó có chỉ số IPIC bằng hoặc lớn hơn 0,7 (WOAH, 2021). (WOAH, 2021). Có sự khác biệt lớn về mức độ độc lực giữa các chủng virus. Bảng 1 tóm tắt chỉ số độc lực của các kiểu độc lực khác nhau thông qua các phương pháp kiểm tra khác nhau (Alexander, 1989 và 1998).
- Dịch niệu đệm (allantoic fluid) được xác nhận dương tính với HA với hiệu giá ngưng kết hồng cầu lớn hơn 1:16 được pha loãng 1/10 trong dung dịch muối sinh lý và tiêm vào não với liều 0,05 mL cho mười gà con SPF 1 ngày tuổi.
- Những con gà được kiểm tra hằng ngày trong 8 ngày, và được chấm điểm mỗi ngày như sau: 0 nếu bình thường, 1 nếu bị bệnh và 2 nếu chết.
- Những con chết sẽ được ghi điểm là 2 cho tất cả các ngày tiếp theo cho đến hết 8 ngày.
-
IPIC được tính bằng điểm trung bình mỗi ngày trên mỗi con gà trong 8 ngày; các chủng virus độc lực cao có điểm tiệm cận mức tối đa 2.0 và các chủng virus độc lực thấp (lentogenic) tiệm cận 0.0.
Tất cả các chủng APMV-1 được coi là thuộc cùng một kiểu huyết thanh (serotype), tuy nhiên, một số biến thể kháng nguyên đã được chứng minh giữa các chủng khác nhau thông qua nhiều phương pháp kiểm tra. Ngay cả khi không có sự khác biệt kháng nguyên rõ ràng giữa các chủng, phân tích di truyền đã trở thành phương pháp chính để đặc trưng hóa và đã thay thế việc sử dụng kháng thể đơn dòng (mAbs) trong việc phân loại các chủng NDV.
XÁC ĐỊNH KIỂU GEN VIRUS
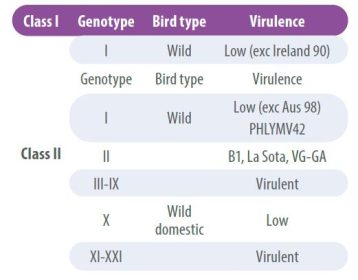
Virus NDV có tỷ lệ tái tổ hợp thấp, tuy nhiên, theo thời gian, đã phát hiện một số khác biệt về kháng nguyên dẫn đến việc phân loại các chủng thành các dòng (lineage) hoặc kiểu gen (genotype). Theo đó, các chủng được chia thành hai nhóm chính: virus lớp I và virus lớp II;
- Virus lớp I có độc lực thấp và thường được tìm thấy ở gia cầm hoang dã.
- Trong khi đó, virus lớp II được phân loại thành nhiều kiểu gen khác nhau và có thể là không gây bệnh hoặc có độc lực cao (Bảng 2).
Việc xác định kiểu gen NDV được thực hiện thông qua giải trình tự toàn bộ gene F, đồng thời giúp xác định độc lực của virus;
- Để xác định các kiểu gen mới, hệ thống phân loại dựa trên khoảng cách tiến hóa trung bình 10% giữa các nhóm di truyền được áp dụng (Dimitrov KM et al 2016; Dimitrov KM et al, 2019).
Sự phát triển của công nghệ giải trình tự thế hệ mới (NGS) đã trở thành một công cụ quan trọng trong nghiên cứu và đặc điểm di truyền của các tác nhân gây bệnh.
- Tuy nhiên, phương pháp này đặc biệt lý tưởng đối với các virus RNA có tốc độ đột biến nhanh, trong đó các yếu tố tiến hóa cũng cần được phân tích (Butt et al., 2019).
Hiện nay, hệ thống phân loại kiểu gen bao gồm thêm ba kiểu gen mới (XIX, XX và XXI), nâng tổng số lên 21 kiểu gen trong nhóm virus lớp II (Dimitrov et al. (2019).
KHẢ NĂNG KHÁNG TÁC NHÂN VẬT LÝ VÀ HÓA HỌC
Là một loại virus có vỏ bọc, virus Paramyxoviridae ở gia cầm rất dễ bị bất hoạt bởi các tác nhân vật lý và hóa học như:
- Nhiệt độ cao,
- Tia cực tím (UV),
- Các quá trình oxy hóa,
- Độ pH và
- Xử lý bằng hầu hết các loại chất khử trùng.
Tuy nhiên, các công bố về thời gian sống sót của virus bên ngoài vật chủ cho thấy có sự khác biệt, phụ thuộc vào nhiệt độ, độ ẩm và môi trường mà virus được kiểm nghiệm (Kinde et al., 2004).
PDF














