Nội dung có ở: English Indonesia (Indonesian) ไทย (Thai) Philipino
Các biến thể của virus viêm túi Fabricius truyền nhiễm: Thách thức đối với vắc xin thương mại?
Bệnh Gumboro, còn được biết đến với tên gọi Viêm túi Fabricius truyền nhiễm (IBD) hoặc Viêm túi huyết truyền nhiễm ở gia cầm, lần đầu tiên được báo cáo tại Delaware, Hoa Kỳ, vào năm 1962. Đây là một bệnh virus gây suy giảm miễn dịch, chủ yếu ảnh hưởng đến gà từ 3 đến 6 tuần tuổi và đã lan rộng trên toàn thế giới.
- Virus gây ra căn bệnh này thuộc chi Avibirnavirus, họ Birnaviridae, và có hai kiểu huyết thanh: I và II.
- Kiểu huyết thanh I đã được phát hiện ở gà, gà mái, bồ câu và gà sao (Kasanga và cộng sự., 2008) nhưng chỉ gây bệnh ở gà và gà mái.
- Kiểu huyết thanh I được chia thành hai phân nhóm kháng nguyên: cổ điển và biến thể, trong khi kiểu huyết thanh II không gây triệu chứng ở gà tây, quạ, đà điểu và vịt (Ogawa và cộng sự., 1998; Yilmaz và cộng sự., 2019).
Kể từ báo cáo đầu tiên, nhiều biến thể của loại virus này đã được xác định, làm phức tạp thêm nỗ lực kiểm soát căn bệnh này. Cho đến những năm 1980, tiêm phòng vẫn hiệu quả trong việc kiểm soát bệnh, với tỷ lệ tử vong ở gà thịt dưới 2%.
Tuy nhiên, do virus tiếp tục đột biến và tái tổ hợp, các biến thể kháng nguyên mới đã xuất hiện, dẫn đến tỷ lệ tử vong cao hơn, ngay cả khi áp dụng các phác đồ tiêm phòng nghiêm ngặt.
Các biến thể này có thể xuất hiện mà không gây triệu chứng rõ ràng, làm chậm tốc độ tăng trưởng và tăng khả năng nhiễm các bệnh thứ phát, gây thiệt hại kinh tế đáng kể cho ngành chăn nuôi gia cầm.
PHÓNG TO CẤU TRÚC VIRUS
- Virus có hình dạng khối đa diện đều (icosahedral), không có lớp vỏ bao, và bao gồm hai đoạn RNA sợi kép thẳng, được đặt tên là A và B.
Đoạn B mã hóa VP1 – một enzyme polymerase RNA của virus, trong khi đoạn A sản sinh các protein capsid pVP2 và VP3, cũng như enzyme phân giải VP4 và VP5 – một protein không cấu trúc có vai trò trong điều hòa và phá vỡ màng tế bào bị nhiễm (Mundt, 1999) (Hình 1).
Trong số các thành phần được đề cập ở trên, protein VP2 đặc biệt quan trọng vì nó quyết định tính kháng nguyên, độc lực và khả năng gây bệnh của virus. Protein này chứa các vùng mà kháng thể có thể liên kết, và khi tiếp xúc với phản ứng miễn dịch, nó có xu hướng đột biến mạnh hơn, khiến vùng này trở nên biến đổi cao (Letzel và cộng sự, 2007).
- Protein capsid VP2 gồm ba vùng riêng biệt: đáy (B – base), vỏ (S – envelope), và phần nhô ra (P – projection).
- Vùng P bao gồm bốn cấu trúc vòng (loop) lộ ra trên bề mặt virus.
- Vòng Pbc (tại các vị trí axit amin 219 và 224) có vai trò trong việc ổn định vị trí nhận biết kháng thể.
- Vùng Phi (các axit amin từ 315–324) được nhận diện bởi các kháng thể trung hòa và là vị trí chính xảy ra đột biến axit amin giúp virus tránh được phản ứng miễn dịch.
- Hai vòng còn lại, Pde (axit amin từ 250–254) và Pfg (axit amin từ 283–287), có liên quan đến khả năng gây bệnh của virus (Jackwood và cộng sự, 2018) ( Hình 2).
Ngoài ra, cấu trúc phân đoạn của bộ gen virus giúp dễ dàng xảy ra hiện tượng tái tổ hợp gen giữa các chủng khi xảy ra đồng nhiễm. Ví dụ, điều này cho phép chủng virus sống từ vắc xin và chủng virus hoang dã có thể trộn lẫn với nhau. Do đó, các đột biến và sự tái tổ hợp góp phần tạo ra sự biến đổi kháng nguyên, từ đó làm giảm hiệu quả của các loại vắc xin thương mại và gây ra những thách thức lớn trong việc kiểm soát dịch bệnh (Gao và cộng sự, 2007).
NHỮNG TIẾN BỘ TRONG HỆ THỐNG PHÂN LOẠI VIRUS
- Từ lần phát hiện đầu tiên vào năm 1962, các chủng không được phân loại riêng biệt vì người ta cho rằng chúng có tính kháng nguyên và độc lực tương tự nhau.
- Tuy nhiên, vào năm 1980, việc phát hiện ra kiểu huyết thanh 2 đã dẫn đến sự xác định các biến thể kháng nguyên (gọi là “biến thể”) cũng như các chủng có độc lực rất cao (gọi là “các chủng rất độc” – vvIBDV).
- Do đó, các chủng được phát hiện trước các biến thể này được phân loại là “các chủng cổ điển”.
- Các phương pháp đặt tên thay thế đã được sử dụng, dựa trên tên của nhà khoa học đầu tiên phân lập chủng (ví dụ: Winterfield, Lukert, Moulthrop, Baxendale), địa điểm phân lập (ví dụ: Del-A, Del-E, MD, OH) hoặc mã số/chữ (ví dụ: STC, D78, G603, S706, 228E).
Tuy nhiên, theo thời gian, các đặc điểm liên quan đến tính kháng nguyên, cấu trúc phân tử và độc lực của các nhóm này đã được phát hiện. Điều này dẫn đến một hệ thống phân loại truyền thống, chia các chủng thành cổ điển và biến thể, trong đó nhóm biến thể được chia nhỏ thành các chủng suy giảm độc lực, độc lực trung bình và rất độc.
Về mặt bộ gen, các chủng IBDV rất độc lực (vvIBDV) có các axit amin đặc trưng tại các vị trí 222 (Ala), 256 (Ile), 294 (Ile) và 299 (Ser) trong trình tự VP2. Về độc lực, so với các chủng cổ điển, vvIBDV thường gây tỷ lệ tử vong cao hơn ở gà không mang mầm bệnh (specific pathogen-free) khi bị nhiễm) (Van Den Berg và cộng sự, 2004). Tuy nhiên, không phải tất cả các chủng rất độc đều thể hiện độc lực cao, cho thấy hệ thống phân loại này vẫn chưa hoàn chỉnh (Jackwood và cộng sự, 2018).
- Sau đó, do sự đột biến và tái tổ hợp liên tục, nhiều chủng mới không thể được phân loại bằng hệ thống truyền thống.
- Do đó, Michel và Jackwood (2017) đã đề xuất một hệ thống phân loại mới dựa trên trình tự axit amin của vùng siêu biến trong VP2. Cách tiếp cận này đã dẫn đến việc xác định 7 nhóm gen (genogroups).
- Tuy nhiên, các nhóm gen này không bao gồm các chủng biến thể mới hoặc các chủng suy giảm độc lực.
- Hơn nữa, do đặc điểm tái tổ hợp của các đoạn gen virus, một hệ thống phân loại chỉ dựa trên VP2 không thể phản ánh đầy đủ sự phức tạp của các nhóm gen virus.

Năm 2021, Wang và cộng sự đã đề xuất một hệ thống phân loại mới xem xét các đặc điểm phân tử của VP1 và VP2, bắt nguồn từ các phân đoạn B và A tương ứng.
- Cách tiếp cận này dẫn đến việc xác định 9 nhóm gen (genogroup) cho phân đoạn A và 5 nhóm gen cho phân đoạn B.
- Đáng chú ý, genogroup A2 bao gồm 4 dòng khác biệt.
- Trong hệ thống phân loại mới này, các kiểu gen A1B1, A2B1, A3B2 và A8B1 tương ứng với các kiểu hình cổ điển, biến thể, rất độc lực và suy giảm độc lực.
SINH BỆNH HỌC VÀ BIỂU HIỆN LÂM SÀNG
Trong quá trình gây bệnh điển hình, virus IBDV xâm nhập vào cơ thể qua đường hô hấp hoặc đường phân-miệng, ban đầu nhân lên trong các đại thực bào và tế bào lympho ở ruột hoặc vùng lân cận.
- Quá trình nhân lên ban đầu này dẫn đến sự xuất hiện của viremia sơ cấp qua tuần hoàn cửa, cho phép virus đến cơ quan đích chính là túi Fabricius.
- Trong túi này, virus hoạt động mạnh mẽ trong các nang và tế bào lympho B, những tế bào đang phân chia tích cực ở gà con non.
- Sự nhiễm bệnh gây thoái hóa và hoại tử các nang, chủ yếu ảnh hưởng đến tế bào lympho B mang IgM+, và dẫn đến sự xâm nhập của các tế bào dị loại (heterophils).
- Các tế bào dị loại này sau đó cũng bị hoại tử và được thực bào.
- Tại các vùng giữa các nang (interfollicular), sự tăng sinh của các tế bào hệ võng nội mô được quan sát, dẫn đến tình trạng teo tiến triển của túi Fabricius (Müller và cộng sự, 2012).
- Mặc dù virus không nhân lên trong tế bào lympho T, nhưng sự chết theo chương trình (apoptosis) của các tế bào này được quan sát thấy ở tuyến ức, và các tổn thương vi thể có thể phục hồi sau vài ngày nhiễm bệnh (Jagdev và cộng sự, 2000).
- Regarding secondary viremia, it begins approximately 11 hours after replication in the bursa.
- Trong giai đoạn này, virus đi vào máu và lan rộng đến thận, cơ bắp và các cơ quan khác, gây ra các triệu chứng lâm sàng như mệt mỏi, lông xù, bỏ ăn và tiêu chảy.
- Trong các trường hợp nghiêm trọng, điều này có thể dẫn đến tử vong (Eterradossi & Saif, 2008).
Virus kích thích tế bào lympho B, làm tăng biểu hiện các gen kháng virus thuộc con đường interferon loại I (IFN), các gen thúc đẩy quá trình chết tế bào theo chương trình (proapoptotic), và các cytokine tiền viêm. Ngoài ra, các protein VP2 và VP5 gây apoptosis ở tế bào lympho B và các tế bào lympho khác. Trong quá trình virus nhân lên, có sự xâm nhập đáng kể của tế bào lympho T vào túi Fabricius, tình trạng này kéo dài đến khoảng 12 tuần sau nhiễm.
- Từ ngày thứ 7 sau khi nhiễm, số lượng tế bào lympho T CD8+ (gây độc tế bào) vượt trội so với tế bào T CD4+.
- Sự gia tăng này thúc đẩy quá trình tiêu diệt tế bào bằng cách phân giải các tế bào biểu hiện kháng nguyên virus và sản sinh các cytokine tiền viêm như IFN-γ.
- Cytokine này kích thích đại thực bào giải phóng nitric oxide, làm tăng tổn thương mô túi (Jagdev và cộng sự, 2000) và góp phần gây mệt mỏi cho các tế bào miễn dịch.
Các biến thể virus gây ra mức tăng cao các cytokine IFN-γ, IL-6, IL-8, IL-18, NLRP3, caspase 1 và TNF-α, thúc đẩy viêm và thay đổi vi môi trường mô. Chiến lược này làm ức chế hoạt động của tế bào lympho B, cho phép virus né tránh phản ứng miễn dịch, dẫn đến tổn thương túi nghiêm trọng hơn và gây suy giảm miễn dịch mạnh hơn so với các chủng cổ điển (Jagdev và cộng sự, 2000; Li và cộng sự, 2023).
- Ví dụ, Li và cộng sự (2023) chứng minh rằng vvIBDV có độc lực cao, khả năng nhân lên mạnh mẽ và năng lực gây tổn thương nghiêm trọng cho túi và các mô khác, dẫn đến tỷ lệ tử vong cao.
- Chủng này lan đến túi Fabricius, hạch ruột, tuyến ức và lách, đồng thời làm thay đổi mức cytokine trong túi.
- Ngược lại, biến thể SHG 19 từ Trung Quốc, được báo cáo vào năm 2020, có khả năng nhân lên thấp hơn và không gây tử vong, nhưng vẫn gây tổn thương nghiêm trọng cho các cơ quan miễn dịch, tương tự vvIBDV.
- Biến thể này gây hoại tử và phân rã mạnh tế bào lympho B, mặc dù những thay đổi này diễn ra chậm hơn khoảng 12 giờ so với chủng độc lực cao.
- Cơ chế chậm này có thể giúp biến thể bài tiết ra ngoài dễ dàng hơn, từ đó có khả năng trở thành chủng gây dịch chủ yếu (Fan và cộng sự, 2020).
THÁCH THỨC ĐỐI VỚI VẮC-XIN THƯƠNG MẠI
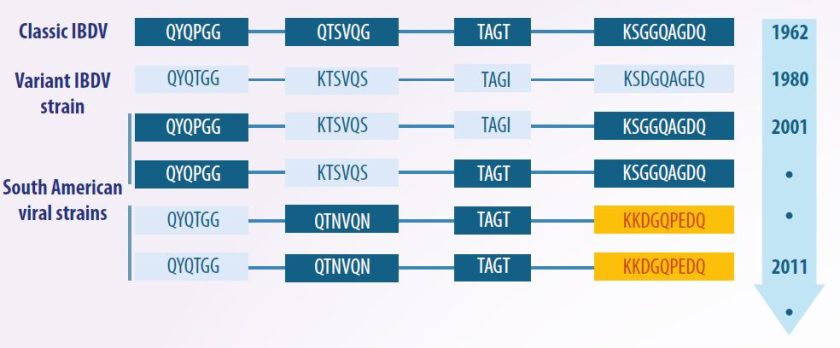
Việc tiêm vắc xin với các kiểu gen khác với virus hoang dã có thể dẫn đến sự đa dạng di truyền trong các chủng virus đang lưu hành. Trong những trường hợp như vậy, hiện tượng tái tổ hợp có thể xảy ra — ví dụ giữa đoạn A của một chủng rất độc lực và đoạn B của một chủng cổ điển — dẫn đến tỷ lệ tử vong lên tới 80% ở gà có tổn thương cấp tính ở túi Fabricius (Pikuła và cộng sự, 2018) (Hình 3).
Hơn nữa, khoảng cách kháng nguyên giữa chủng virus hoang dã và chủng dùng trong vắc xin khiến các biến thể có thể không bị kiểm soát hiệu quả bởi các vắc xin serotype 1 truyền thống. Do đó, hiện nay khuyến nghị rằng việc sản xuất vắc xin chống lại IBDV nên bao gồm việc lập bản đồ kháng nguyên – một phương pháp tính toán để xác định khoảng cách kháng nguyên giữa các chủng. Kỹ thuật này đã được áp dụng thành công đối với virus cúm ở người và ngựa. Mặt khác, điều quan trọng là cần đánh giá khả năng bảo vệ chéo trong quá trình phát triển vắc xin để đảm bảo hiệu quả (Boudaoud và cộng sự, 2016).
KẾT LUẬN
- IBD vẫn là một thách thức lớn đối với ngành công nghiệp gia cầm do virus có khả năng đột biến nhanh, tái tổ hợp di truyền và sự xuất hiện của các biến thể mới có độc lực cao.
- Các biến thể này gây suy giảm miễn dịch nghiêm trọng, tỷ lệ tử vong cao và làm tăng nguy cơ nhiễm trùng thứ phát, mặc dù đã có các nỗ lực tiêm phòng.
- Tính phức tạp về mặt di truyền của virus, đặc biệt là ở protein VP2, khiến việc phát triển vắc xin hiệu quả trở nên khó khăn, vì sự thay đổi kháng nguyên có thể làm suy giảm hiệu quả của vắc xin.
- Sự tiến hóa liên tục của virus đòi hỏi các chiến lược tinh vi hơn, chẳng hạn như lập bản đồ kháng nguyên và đánh giá khả năng bảo vệ chéo, nhằm cải thiện thiết kế vắc xin và nâng cao hiệu quả kiểm soát căn bệnh gây thiệt hại kinh tế này.
*Các tài liệu tham khảo có thể được cung cấp theo yêu cầu từ tác giả