Epidemiologia da Doença de Newcastle
21 jun 2024
Epidemiologia da Doença de Newcastle
Epidemiologia da Doença de Newcastle CONCEITUAÇÃO Doença viral infecciosa altamente transmissível, pioneiramente descrita em 1926 em Java/Indonésia e em […]
- CONCEITUAÇÃO
Doença viral infecciosa altamente transmissível, pioneiramente descrita em 1926 em Java/Indonésia e em Newcastle/Inglaterra, com diferentes intensidades de severidade em galinhas.
- ETIOLOGIA
Agente etiológico: O vírus responsável pela Doença de Newcastle é um RNA vírus, pertencente á família Paramyxoviridae, gênero Paramyxovirus que comporta até o momento 9 sorogrupos identificados de PMV-1 até PMV-9, classificação esta realizada em função da relação antigênica na reação de Inibição de Hemaglutinação e raramente ocorrem reações cruzadas entre os sorogrupos.

O vírus da DNC pertence ao MVP-1.e a manifestação da patogenicidade varia de acordo com a susceptibilidade ligada à espécie animal. Assim, galinhas são mais susceptíveis que pombos e gansos. Em galinhas, a patogenicidade varia segundo o patótipo do vírus, dose infectante, via de penetração ou inoculação do vírus, idade e condições do meio ambiente.
A maior letalidade é observada entre jovens que podem morrer antes do aparecimento de sintomas. Portanto, em se tratando do vírus da DNC é importante reconhecer as diferentes estirpes em termos de alta e de baixa patogenicidade para galinhas e talvez de forma mais pertinente em estirpes endêmicas e epidêmicas (PaulillO & Doretto Jr1, 2000).
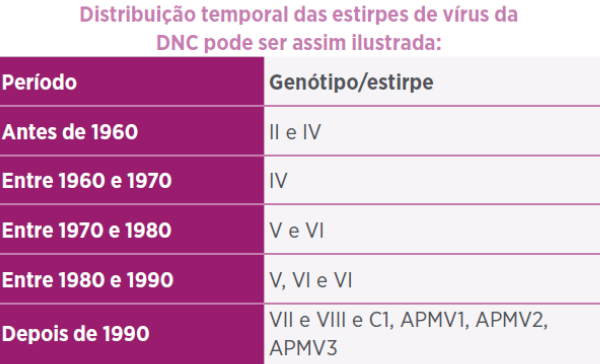
- EVOLUÇÃO VIRAL E ESTIRPES VIRAIS IDENTIFICADAS EM DIFERENTES PAÍSES DO MUNDO
- GERAL
EVOLUÇÃO DO PARAMYXOVIRUS TIPO 1 DE POMBO (Ujvari et al.2, 2003): com base em estudo de isolados de pombos de 16 países (1978 – 2002) permitiu classificar no sub-grupo VIb/1 do genótipo VI da estirpe de galinha. Os diferentes graus de diversidade genética observada no início de epidemia sugerem prolongado período de infecção do vírus tipo-pombo antes da emergência da epidemia de 1980’ em galinhas. Revelada relação genética da epidemia de 1970’com estirpe do Sudão sugerindo que o PPMV-1 tenha se originado da África.
-
-
- Sub-grupo VIb/1: Iraque, Europa (focos mais antigos), América do Norte e Europa (focos mais recentes) são estirpes que surgiram e circularam nas últimas décadas.
- Sub-grupo EU/ea e estirpe América do Norte (NA): responsáveis por epidemias na década de 1980”.
- Sub-grupo EU/re responsável pelo episódios de 1990’.
-

-
- EPIDEMIAS E ISOLADOS NA ÁSIA
-
-
- Epidemias em Taiwan (Yang et al.3, 1999; TSAI et al.4, 2004)
- – 1969, 1984 e 1995: por vírus relacionado com episódio do Oeste Europeu;
- – 1969 foi por genótipo semelhante ao III e temporariamente denominados X e VIh X e VIh;
- – 1984 e 1995 e o episódio de 1998 foram pelo tipo VII (VIb, VIh, VIIa e X);
- – 1995-1996: velogênica dos genótipos VIIa ou VIII e com relação epidemiológica entre estirpes de 1969 e 1984 e sem relação entre 1969 e 1984 com 1995-1996.
- Epidemias na China
- – Entre 1979 e 1999: (LIANG5 et al., 2002) genótipos VIIa e VIII predominantes, na época, na África do Sul.
- – Entre 1985- 1991: isolados de galinhas e gansos e caracterizados como velogênicos dos genótipos VI (f e g), VII (a, b, c, d, e) (LIU et al.6, 2006).
- Epidemias na Rep. China e em Taiwan de 1996-2000 (YU et al.7, 2001) foram os genótipos novos VIIc e VIId (velogênico viscerotrópico e velogênico neurotrópico) e genótipo VIb (mesogênico). As epidemias da China e Taiwan eram relacionadas e a de 1990 (Ásia, Oriente Médio, África e Europa) foi parte integrante da 4ª pandemia.
- Isolados na república da Coreia:
- – 1995: era VIIa e mais semelhante ao de Taiwan do que do Europeu e fora recém introduzido.
- – 1988-1999: estudos genéticos indicaram que a maioria dos isolados pertenciam ao cluster do genótipo VI e distante de outros isolados e foi provisoriamente denominado VIf com evidencias de que estava circulando há décadas com infecção (inaparente). Isolado de 1995 foi VIa (mesmo do Oeste Europeu) e VIIa teria surgido recentemente na Coréia. (KWON et al.8, 2003)
- Isolados no Japão (1997-2000): virus lentogênico em gansos infectados a partir de aves aquáticas migratórias que pode ser precursor de velogênica isolado apenas em 2000. (Shengqing et al.9, 2002).
- Epidemias em Taiwan (Yang et al.3, 1999; TSAI et al.4, 2004)
-
-
- EPIDEMIAS E ISOLADOS NA ÁFRICA
Estirpe e estudo filogenético das epidemias entre 1990 e 2002 na África (Abolnik et al.10, 2004):
-
-
- – Isolados entre 1990-2002 – todas as lentogênicas eram de origem de vacina comercial e as mesogênicas eram avirulentas.
- – Epidemia de 1990/1991 causada por vírus endêmico desde 1960 (genótipo VIII) e ocasionalmente isolado em 2000 e originário do Extremo Oriente.
- – Epidemia de 1993/1994 foi pelo genótipo VIIb que persistiu até 1999 oriundo do Extremo Oriente.
- – Epidemia de 1999/2000 causada pelo genótipo VIId e oriundo muito provavelmente do Extremo Oriente como foram as 2 epidemias anteriores.
-
-
- EPIDEMIAS E ISOLADOS NA EUROPA
- Alemanha: Epidemias entre 1939 a 1995 (Wehmann et al.11, 2003):
-
- – Antes de 1970 – sub-tipo IVe do genótipo IV, mesmo que circulou na Europa até final 70’.
- – A partir de 1970 – estirpe like-Essex70, sub-tipo do genótipo V que teria se originado do Oeste Europeu.
- – No início de 1980’ em galinhas – sub-tipo VIc do genótipo VI
- – De 1993-1995 – genótipo VII1 simultaneamente à epidemia no Extremo Oriente.
-
- Bulgária: Epidemia (da pandemia da Europa) de 1959 e 1996 (Czegledi et al.12, 2002):
-
- – 1ª pandemia: pelo genótipo IV e continuou em cena até 1980’ alternando com genótipo II.
- – 1980’: pelo genótipo V teve origem em psitacídeos da América do Sul e persistiu até fins de 1980’.
- – 1968-1970 e entre 1968-1970: pelo genótipo VI;
- – 1984: pelo genótipo VIIb associado com epidemias do Leste Europeu
-
- Bosnia-Herzegovina, Croácia, Eslovênia e Iugoslávia entre 1972 E 2002 (Wehmann et al.13, 2003) foram os seguintes isolados:
-
- – V (genótipo exótico): Isolados das Vb1: dominante na Bulgária desde 1970’e disseminada a antiga Iugoslávia.
- – Vb2: variante que ocorre em países vizinhos desde 1970’e que poderia ter sido a causa da epidemia na Iugoslávia e que esteve presente até 1980’.
- – Vb3 e Vb4: poderiam ter sido identificadas somente após 1987. Assim, os surtos na Iugoslávia foi parte da onda pelo genótipo V que iniciou no oeste europeu em 1970 e que se tornou endêmica.
-
Todas as variantes se disseminaram entre os paises e as variantes Vb3 e Vb4 podem ter-se desenvolvido durante o período endêmico.
- Dinamarca: Epidemia de 1996 em faisões de vida livre: estirpe C1 virulenta da APMV-1 (Jorgensen et al.14, 1999).
- Austrália: Epidemia em 1998-2000 devido ao mesmo vírus endêmico que fora isolado de pintinhos (Gould et al.15, 2001)
- França: Epidemia na em pombos (2000’): estirpe virulenta de aPMV-1 (Barbezange & Jestin16, 2003).
- Espanha: Isolado (2000) de aves de caça (partridge) com Ac contra aPMV (2 e 3) indicando circulação desses vírus em aves de vida livre e dispensando vacinação porque não foi detectado tipo 1. (Hoefle et al.17, 2001).
- Itália: Isolados de pombos pertencente à estirpe APMV1 e variante PPMV1 sugerindo que várias estirpes circulam na mesma população de pombos selvagens. (Terregino et al.18, 2003) e intimamente relacionado com isolados (grupo C1) da Inglaterra, Escandinávia e Sudeste europeu sugerindo circulação do vírus na Europa nos últimos 5 anos a contar de 2001 (Cattoli et al.19, 2001).
-
- EPIDEMIAS E ISOLADOS NA AMÉRICA DO NORTE
- NOS EUA:
- Não foi isolado no norte do Texas em galinhas do prado e nem em perus silvestres do Rio Grande/Texas (Peterson et al.20, 2002; Peterson et al.21, 2002).
- Isolados no Alabama e Mississipi de cormorantes: Ac presente em cormorantes de crista dupla migratórias. (Farley et al.22, 2001).

- Epidemia de 1992 em cormorante de crista dupla: em 7 estados do no norte dos USA (cormorante) e em 3 províncias do Canadá (pelicanos) revelando a importância de aves silvestres como importantes reservatórios para galinhas domésticas (Glaser et al.23, 1999).
- Epidemia de 2002 a 2003: na Califórnia, Nevada, Arizona e Texas, por estirpe virulenta que apresentou relação estreita com estirpe ocorrida em 2002 no México e América Central (tipo 1) e o isolado do Texas de 2003 com estreita relação com isolado do México de 2002. Surtos nos USA vieram de países circunvizinhos indicando necessidade de se intensificar medidas de vigilância de aves comerciais e não comerciais (Pedersen et al.24, 2004).
- Hospedeiros:
Muitas espécies de aves domésticas e silvestres são hospedeiros naturais do VDN sendo as mais importantes, galinhas, perus, patos, gansos, faisão, aves psitacinas, aves migratórias. Psitacídeos e muitas espécies de aves silvestres são mais resistentes que outras como os galináceos e atuam, na epidemiologia da doença, como portadores. O estado de portador pode existir entre psitacídeos e outras aves silvestres.
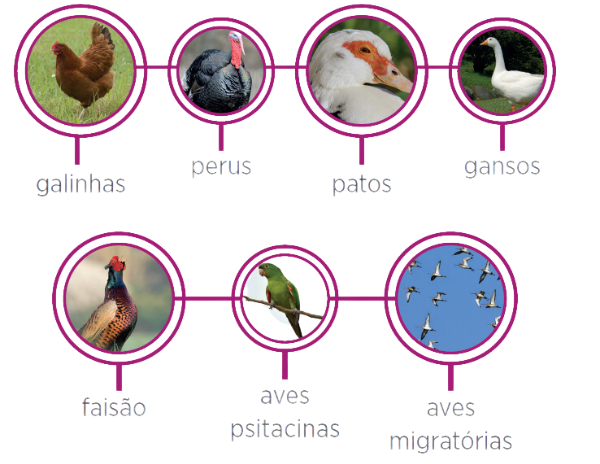
- AVES DE IMPORTÂNCIA EPIDEMIOLÓGICA:
- Pequena importância ou não foram detectados infectados:
Passarinhos: isolado patótipo lentogênico do APMV1 na Ilha de Helgoland (Mar do Norte) indicando pequena importância dessas aves como potenciais reservatórios (Schnebel et al.25, 2005).
-
- Importância como reservatório:
Citações sobre a importância epidemiológica de aves de vida livre incluindo silvestres como reservatórios em potencial para as criações comerciais de galinhas principalmente. Tem sido particularmente estudadas:
Galinhas de fundo de quintal:
PARA SEGUIR LENDO REGISTRE-SE É TOTALMENTE GRATUITO
Acesso a artigos em PDF
Mantenha-se atualizado com nossas newsletters
Receba a revista gratuitamente em versão digital
CADASTRO
ENTRE EM
SUA CONTA
ENTRAR
Perdeu a senha?