
Inmediatamente después del nacimiento de los pollitos, comienza el proceso de colonización microbiana del intestino, principalmente por bacterias del entorno ambiental, que son ingeridas de forma permanente a través de la alimentación.
De esta manera, se va conformando un ecosistema microbiano, compuesto por una población bacteriana diversa y dinámica, con importantes funciones. Entre ellas, proporcionar una protección de la mucosa intestinal frente a bacterias patógenas y desempeñar un papel esencial en el normal desarrollo y homeostasis del sistema inmune a este nivel.

En esta etapa, donde la microbiota se está desarrollando y los mecanismos de defensa se hallan en proceso de maduración, es cuando las aves se encuentran más susceptibles y expuestas a padecer ciertos trastornos gastrointestinales, principalmente infecciones por bacterias enteropatógenas.
Al mismo tiempo, estas enfermedades pueden aparecer durante otras etapas productivas, por ejemplo, cuando los animales se enfrentan a situaciones de estrés o debido a la presencia de otros factores de riesgo.
Dentro de este grupo de bacterias, las que más comúnmente atentan contra la salud intestinal de las aves son Salmonella, E.coli, Clostridium, entre otras.
Estas bacterias utilizan sus factores de virulencia para llevar a cabo sus mecanismos de patogenicidad, y, a su vez, le otorgan un gran poder de contaminación y resistencia ambiental, así como la capacidad de evadir la respuesta inmune del huésped para generar daño.
Inmunidad en la mucosa intestinal
La mucosa intestinal es una de las mayores áreas inmunológicas del organismo, comprende una extensa superficie de contacto e interacción entre el huésped y el entorno.
Es un lugar de reconocimiento antigénico, de los distintos microorganismos que ingresan y recorren por el tracto digestivo, con el fin de generar tolerancia frente a bacterias inocuas y una respuesta inmune frente a patógenos.
El tejido linfoide asociado al intestino (GALT) contiene más del 70% del total de células inmunitarias del cuerpo y aproximadamente 80% de todas las células plasmáticas, productoras de inmunoglobulinas A (IgA). (2).
La inmunidad innata:
Proporciona la primera línea de defensa contra la infección mediante sus cuatro tipos de barreras: anatómicas, fisiológicas, fagocíticas e inflamatorias (1).
La mucosa intestinal:
Constituye una eficiente barrera protectora, conformada por la integridad de su epitelio, una doble capa de moco que lo recubre y un microbioma que compite por espacio y nutrientes contra microorganismos patógenos.
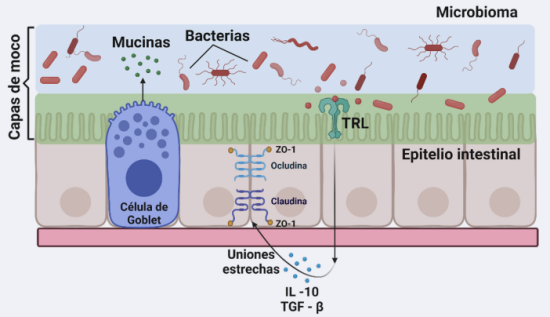
Las células epiteliales del intestino, conocidas como enterocitos, presentan varias propiedades, entre ellas, una continuidad dada por sus uniones estrechas y la capacidad de producir citoquinas que mantienen un estado de homeostasis.

Las uniones estrechas son reguladas por citoquinas anti-inflamatorias, como la IL-10 y TGF-β, que incrementan la resistencia de las uniones, disminuyendo la permeabilidad intestinal al pasaje de macromoléculas.
A su vez, el daño tisular que causa un microorganismo patógeno invasor, induce una secuencia compleja de eventos conocidos como respuesta inflamatoria.
El resultado final de la misma puede ser la eliminación del patógeno por componentes del sistema inmunitario innato o la activación de una respuesta inmune específica al microorganismo.
Muchas de las moléculas implicadas en la inmunidad innata tienen receptores que reconocen motivos estructurales altamente conservados, sólo dentro de las especies microbianas, denominados receptores de reconocimiento de patrones (PRR).
Los patrones moleculares asociados a patógenos (PAMPs) reconocidos por este tipo de receptores incluyen combinaciones de azúcares, ciertas proteínas, moléculas portadoras de lípidos y algunos motivos de ácidos nucleicos.
La capacidad de estos receptores para distinguir entre lo propio y lo extraño es muy eficiente, ya que el patrón molecular al que se dirige el receptor se encuentra solo en el patógeno y nunca en el huésped, siendo esta capacidad una característica importante de la inmunidad innata (1).
Los receptores tipo Toll (TLR) forman parte del sistema inmune innato y reconocen patrones expresados por diversos microorganismos. Desempeñan un papel central en la respuesta inmune innata y son importantes reguladores de la inmunidad adaptativa.
Tienen funciones clave en la detección de microorganismos, las fases iniciales de las respuestas inmunitarias a los patógenos y en el inicio de respuestas inflamatorias (2).

Estos receptores son proteínas transmembrana que se encuentran tanto en células del sistema inmune, como macrófagos o células dendríticas, así como también en células del epitelio intestinal.
Están conformadas por un ectodominio en forma de herradura, donde se produce el contacto directo entre la superficie del receptor y las moléculas microbianas específicas, el dominio transmembrana y un dominio intracelular que permite la transmisión de las señales (3).
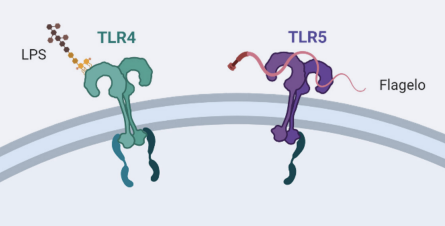
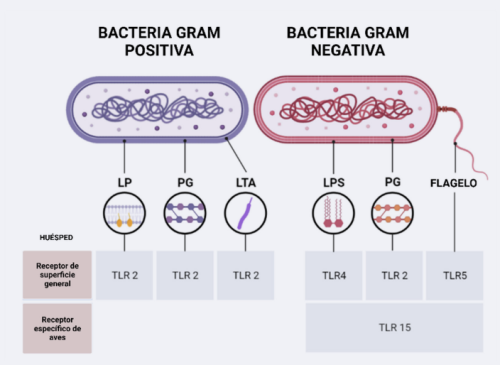
Reconocen diversos patrones moleculares asociados a patógenos (PAMPs) como los lipopolisacáridos (LPS) y peptidoglicanos (PG) de la pared celular bacteriana, así como también la flagelina, el componente proteico de los flagelos.
La familia de TLR aviares consta típicamente de diez receptores, cada uno adaptado a distintos ligandos, de los cuales algunos pertenecen a los TLR de un solo dominio (TLR3, TLR5, TLR7, TLR15 y TLR21) y otros a los TLR de tres dominios (TLR1A, TLR1B, TLR2A, TLR2B y TLR4 (3).
La interacción entre los TLRs y los PAMPs, origina una secuencia de eventos y la activación de diferentes vías de señalización que culminan en la producción de factores de transcripción, que inducen la expresión de genes que son clave para desencadenar una respuesta inmunitaria y la subsiguiente estimulación de la inmunidad adquirida (3).
Se pudo observar, mediante la estimulación de TLR4 ante el reconocimiento del LPS, la inducción de la síntesis de la proteína ZO-1, que fortalece las uniones del epitelio, disminuyendo la permeabilidad paracelular (4).
A su vez, la detección de productos bacterianos a través de TLR, aumenta la producción y densidad de la capa de moco que recubre la mucosa intestinal, limitando la interacción directa de las bacterias comensales con el epitelio y la generación de inflamación espontánea, al mismo tiempo que protege de la invasión por bacterias patógenas (4).

El epitelio intestinal, cuando se halla en un estado normal e íntegro, va produciendo citoquinas inmunoestimuladoras, para mantener un estado de homeostasis. Cuando los receptores tipo toll (TLR) epiteliales reconocen moléculas microbianas de las bacterias comensales, secretan una diversidad de sustancias, entre las cuales se encuentra el TGF-β, que suprimen las respuestas inflamatorias, contribuyendo a la inducción de la tolerancia inmunológica (4).
Tras la detección de ciertos PAMPs, las vías de señalización de los TLR estimulan la secreción y activación de citoquinas proinflamatorias, como TNF-α. De esta forma, se genera una reacción inflamatoria necesaria para la destrucción bacteriana y al mismo tiempo, presenta un efecto protector y de reparación de tejidos.
La interleuquina 8 (IL-8) es fundamental para el reclutamiento de células inmunes, como macrófagos, células dendríticas, neutrófilos, entre otras, al sitio de inflamación, con el fin de contribuir a la eliminación de las bacterias patógenas (4).
Mediante el estímulo de los TLR de las células dendríticas que residen en la lámina propia intestinal, se liberan citoquinas, como el TGF-β, que cooperan para inducir el cambio de isotipo en linfocitos B de la mucosa intestinal para la producción de anticuerpos IgA secretoria (IgAs), para ser transportada hacia la luz intestinal.
La IgAs presenta características relevantes, como ser resistente a las proteasas intestinales y no inducir inflamación. Otorga mecanismos de protección en la mucosa, neutralizando toxinas y receptores bacterianos, así como moléculas inflamatorias de origen microbiano, como sería el ejemplo del LPS. Simultáneamente, la presencia de IgAs inhibe la unión de bacterias en la superficie epitelial (5).
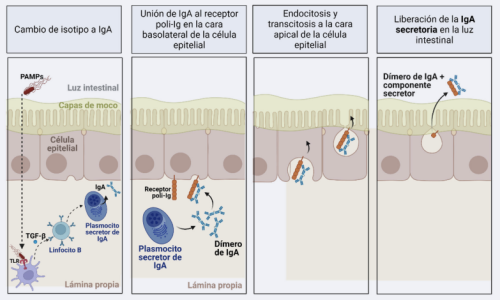
Los mecanismos de inmunidad innata presentes a nivel de la mucosa intestinal desarrollan una actividad inmunológica permanente, al ser el primer lugar de contacto con los principales antígenos bacterianos del medio ambiente, manteniendo una homeostasis intestinal que protege y controla ante la colonización e invasión por enteropatógenos.
GAMAXINE®
Aditivo natural elaborado a base de cepas inactivadas de Bacillus Subtilis y metabolitos derivados de su fermentación, potenciado con el agregado de Manano-oligosacáridos (MOS) de la pared de levaduras.
Las moléculas presentes en GAMAXINE® ayudan a equilibrar la microbiota intestinal, disminuyendo la carga de enteropatógenos y por lo tanto, los niveles de excreción al ambiente.
Mecanismos de acción
1) Disminuye la inflamación intestinal
– Mediante la producción de una citoquina antiinflamatoria (TGF-β), disminuye la permeabilidad intestinal y el pasaje de bacterias hacia el interior de la mucosa.
– Reduce el gasto energético que se genera por los procesos inflamatorios.
2) Fortalece la integridad del epitelio intestinal
– Induce la síntesis de proteínas que permiten que las uniones estrechas del epitelio se encuentren más unidas (ZO-1).
– Aumenta la producción de mucina (MUC– 2), el mayor componente de la capa protectora de mucus intestinal.
3) Modula la respuesta inmune innata
Estimula receptores TLRs específicos, como los TLR 1-2, 4, 5 y 15, que desencadenan una respuesta inmunomoduladora asociada a bacterias, favoreciendo:
El reclutamiento de células inmunes a la mucosa, por medio de la IL-8.
La neutralización de enteropatógenos, mediada por la producción de IgA secretoria (sIgA).
Fue desarrollado para fortalecer el SISTEMA INMUNE DE LAS AVES, y así mejorar su capacidad de responder a los principales desafíos provocados por enteropatógenos.
Su efecto protector de la SALUD INTESTINAL, permite lograr una óptima productividad y lo convierte en una opción viable para reemplazo de los antibióticos.
Referencias bajo consulta al autor

Materias Primas
Suscribete ahora a la revista técnica de avicultura
AUTORES
Comunidad de bacteriófagos en el ambiente
Gary García-Espinosa Janeth Gómez García
La influencia de la luz en el bienestar de las gallinas ponedoras
Édina de Fátima Aguiar
¿Es posible manejar los crecimientos en granjas sin hacer grandes inversiones para su movilización en los galpones de pollos?
Eduardo Cervantes López
Temporización de los paneles de enfriamiento evaporativo
Michael Czarick
Aplicaciones de impedancia bioeléctrica en la producción avícola
Edgar O. Oviedo-Rondón
Cobb-Vantress celebra 10 años de compartimentación de planteles avícolas con la validación de seis países latinoamericanos
Equipo Técnico Cobb
Estrategias de Bioseguridad Integrales para Control de la Influenza Aviar de Alta Patogenicidad: Vacunación Estratégica y Monitoreo Zoonótico en Aves Silvestres
MVZ. Cesar Isaac Ascencio Pérez MVZ. José Alejandro Jiménez Ramírez
Crina® Poultry Plus, una herramienta para la salud avícola con efectos sobre el desempeño productivo y la salud intestinal
Equipo Técnico DSM-FIRMENICH
Factores de estrés invisibles: Cuando los desafíos no visibles limitan el rendimiento
Equipo Técnico A&P Nutrition
Optimizando la nutrición del pollo de engorde moderno – Parte I
Xavier Asensio Dávila
Métodos clave para preservar el color amarillo del pollo
Equipo Técnico BAADER