Salud Animal
VAXXITEK® HVT+IBD: 25 años de eficacia, seguridad y rentabilidad
Para leer más contenidos de aviNews España Diciembre 2024
Salud Animal
Para leer más contenidos de aviNews España Diciembre 2024
Corría la primavera del año 2.000 cuando, dentro de estudios pre-registro, se usó por primera vez, en varias granjas de broilers comerciales de Estados Unidos, la primera vacuna vectorial de la historia en el sector avícola.
La revolucionaria vacuna VAXXITEK® HVT+IBD
VAXXITEK® HVT+IBD es un virus de Marek del serotipo 3 (herpesvirus de pavo=HVT), naturalmente apatógeno como vector, al que se le ha insertado en una región no esencial de su genoma, el gen que codifica la proteína capsular VP2 del virus de Gumboro.
El virus de Marek se empieza a replicar, inmediatamente después de su aplicación, en diferentes células del organismo, expresando y liberando proteína VP2.
Las aves generan rápidamente anticuerpos anti-VP2 que no son neutralizados por los anticuerpos maternos.
VAXXITEK HVT + IBD, al ser un virus de Marek, no interfiere ni genera ningún daño en la bolsa de Fabricio, al contrario que las vacunas vivas (convencionales o de inmunocomplejos).
Las vacunas en base a virus vivo de Gumboro son desarrolladas atenuando cepas virulentas de campo mediante pases en cultivos celulares.
Estos virus vacunales inician su replicación masiva en la bolsa de Fabricio cuando los anticuerpos maternos en sangre son lo suficientemente bajos para permitir su replicación.
Esta replicación del virus, genera daños en los folículos linfoides de la capa mucosa de la bolsa de Fabricio.
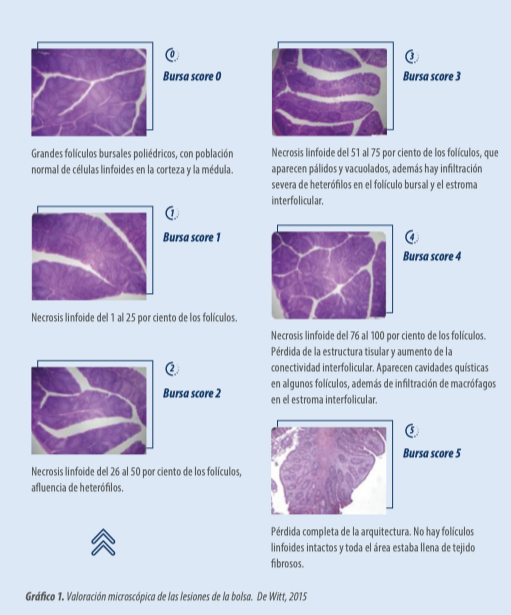
El daño bursal histológico observado en aves vacunadas con cepas intermedias plus puede alcanzar una puntuación (bursa score) de 3,25 (ver Tabla 1).

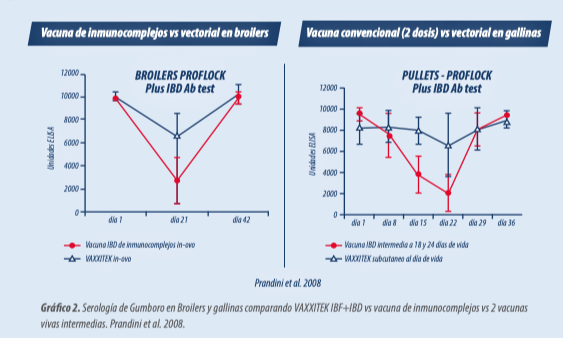
Este daño bursal causado por las vacunas vivas de Gumboro interfiere en la fisiológica migración de los linfocitos B maduros desde la bolsa de Fabricio a los órganos linfoides secundarios:
el bazo, glándula de Harder, tejido linfoide asociado a los bronquios (BALT) y tejido linfoide asociado al intestino (GALT).
Este daño linfocitario causa una reducción de los linfocitos circulantes en sangre (Rautenschlein et al., 2011), reducción de anticuerpos frente a Newcastle (Prandini et al, 2016) y reducción de la respuesta celular (EL Garch et al. 2015).
Una historia de éxito
VAXXITEK® HVT+IBD se ha convertido en la vacuna de Gumboro de referencia mundial. Es protectiva frente a cepas de campo de Gumboro muy virulento y subclínico. Con la experiencia de 100.000 millones de aves (hasta el 2018) en 75 países. Más de 100 publicaciones científicas abalan su eficacia, seguridad y rentabilidad.
Escenario de poca prevalencia
En un escenario de poca prevalencia de Gumboro clínico/subclínico, diferentes estudios comparativos de VAXXITEK® HVT+IBD vs vacunas vivas atenuadas de Gumboro, tanto en el extranjero (Herrmann et al, 2011; Tang et al, 2011; Delquigny et al. 2019) como en España (Castro et al., 2013; Garcés et al., 2010), han visto que VAXXITEK® HVT+IBD, al preservar la Bolsa de Fabricio fisiológica, se logra una mejor base inmunitaria y trae como resultado:
Mejora de los resultados productivos:
Mejora de los resultados de calidad de la canal:
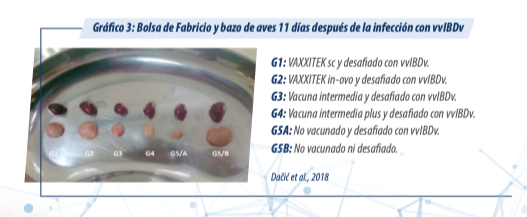
En la proteína VP2, están los epítopos responsables de la generación de anticuerpos neutralizantes, por tanto, VAXXITEK® HVT + IBD genera una respuesta inmune protectiva contra los patotipos clásicos (Wong et al, 2009), variantes (Montiel et al., 2010) y muy virulentos (Lemiere et al., 2013, Dačić et al., 2018) del virus de Gumboro. Ver Gráfico 3.
VAXXITEK® HVT + IBD, al no ser un virus vivo de Gumboro, logra una menor circulación viral en granja, lo que reduce la posibilidad de reordenamientos (intercambio de segmentos génicos) entre cepas vacunales y de campo.
No todas las vacunas vectoriales se desarrollan de la misma forma
La elección del lugar de inserción del casete de expresión VP2 dentro del genoma del virus HVT de Marek es un factor crítico que influye en la capacidad de replicación del virus HVT; y por tanto, influye en el tiempo necesario para que la vacuna vectorial genere el inicio de la inmunidad protectiva.
Otro factor crítico es el sentido de la inserción, es decir a la orientación de un gen insertado en relación con los otros genes del virus HVT de Marek.
Conclusiones:
