Vacunas vectoriales HVT en avicultura
Para leer más contenidos de aviNews España
Para leer más contenidos de aviNews España
Las vacunas vectoriales o vacunas recombinantes son vectores (un virus o una bacteria) que expresan antígenos exógenos. Para ello, se insertan uno o más genes que codifican antígenos, generalmente proteínas, en el ADN del vector. Así, cuando el vector replica en el huésped, no sólo expresa sus proteínas propias sino también las de los genes insertados.
Vacunas vectoriales HVT en avicultura
Se han desarrollado y comercializado vacunas basadas en diferentes vectores en avicultura. Los dos vectores que mayoritariamente se han utilizado para estas vacunas comerciales son dos:
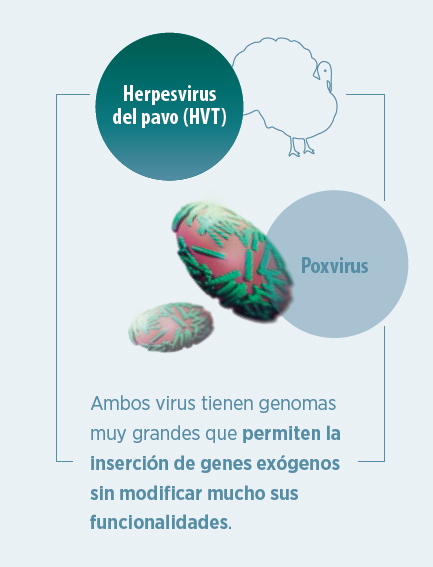
La inmunidad frente a Poxvirus es esencialmente humoral, siendo los anticuerpos generados tras el contacto o infección altamente neutralizantes, lo que nos conlleva dos problemas:
Poxvirus no es un vector adecuado para su administración in ovo.
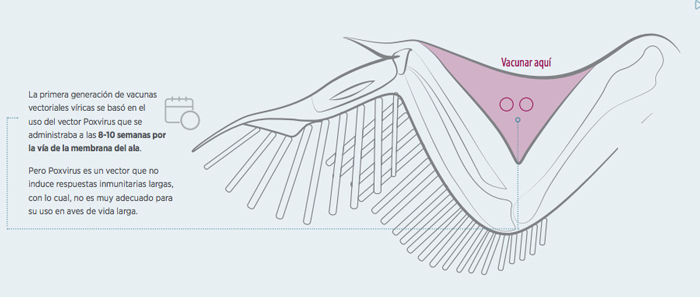
La primera generación de vacunas vectoriales víricas se basó en el uso del vector Poxvirus que se administraba a las 8-10 semanas por la vía de la membrana del ala. Pero Poxvirus es un vector que no induce respuestas inmunitarias largas, con lo cual, no es muy adecuado para su uso en aves de vida larga.
A principios de los años 90 se describió por primera vez el uso del herpesvirus aviar como un vector vírico vivo para la expresión de antígenos heterólogos (Morgan et al., 1992; Sondermeijer et al., 1993). Al estudiar y caracterizar el genoma completo de HVT, se identificaron sitios de este genoma donde potencialmente se podían integrar de forma estable porciones de ADN exógenos, sin que se afectase la capacidad del virus de replicarse en el huésped y de establecer una infección virémica en linfocitos.
Estimulación de la inmunidad frente al inserto mediante las vacunas recombinantes en HVT
Las vacunas vectoriales basadas en HVT son capaces de inducir tanto inmunidad sistémica humoral como celular frente a los antígenos insertados. Por lo general, una de las características de la respuesta inmune generada por vacunas vectoriales HVT es que el inicio de la inmunidad se produce con un poco de retraso.
Así, la mayoría de las vacunas vectoriales HVT comercializadas muestran el inicio de la inmunidad frente al inserto no antes de las 2-3 semanas.
En la Figura 1, se muestra una comparación en la detección del porcentaje de aves positivas frente a ILT tras la vacunación al día de vida con una vacuna vectorial rHVT-ILT con dos kits, un kit clásico (Infectious Laryngotracheitis Antibody Detection kit; Biochek) y un kit específico (IDVET-ID Screen ILT gI Indirect; IDVET). Se puede observar como el kit específico permite detectar antes un mayor porcentaje de aves positivas, y mayores títulos, dado que detecta específicamente los anticuerpos generados por la vacuna vectorial.
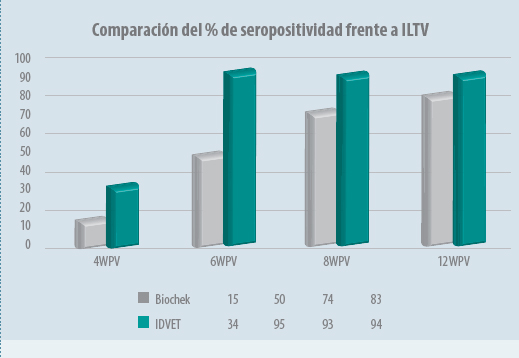
Figura 1a. Comparación del porcentaje de seropositividad frente a ILTV a distintas semanas tras la vacunación con rHVT ILT al día de vida, obtenido con los kits de ELISA de IDVET y Biochek
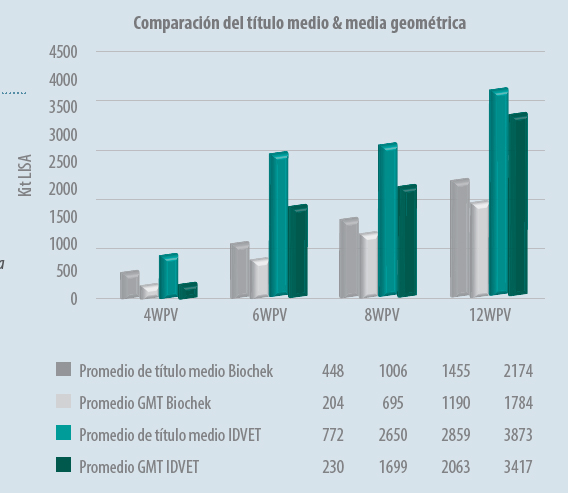
Figura 1b. Comparación del título medio y media geométrica obtenido con los kits de ELISA de IDVET y Biochek a distintas semanas tras la vacunación con rHVT ILT al día de vida
También hay que tener en cuenta que el inicio de la protección no tiene por qué ir ligado a la respuesta serológica. El perfil de seroconversión observado tras la vacunación con una vacuna vectorial rHVT-ILT utilizando un kit específico (tapizado con una de las dos proteínas insertadas en la vacuna), indica un inicio de la respuesta humoral hacia las 4 semanas post vacunación, alcanzando el máximo entre las 8 y 12 semanas post vacunación (Figura 2). Pero por el contrario, la protección completa está demostrada a las 4 semanas post vacunación.
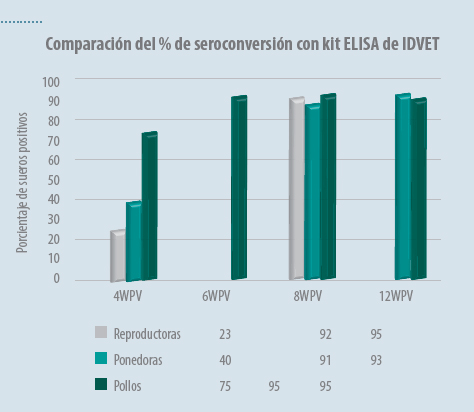
Figura 2. Comparación del porcentaje de seroconversión obtenido con un kit ELISA de IDVET (IDVET-ID Screen ILT gI Indirect) en diferentes tipos de ave, reproductoras pesadas, ponedoras y pollos de crecimiento lento, vacunados al día de vida con rHVT ILT
Es importante mencionar que dentro de la respuesta humoral, las vacunas vectoriales rHVT que incorporan antígenos inhibidores de la hemoaglutinación (HI) generan títulos de anticuerpos de HI más bajos generalmente que las vacunas inactivadas, siendo entonces recomendable utilizar el antígeno homólogo a la hora de evaluar esta respuesta en el test HI, para conseguir una mayor sensibilidad (Suárez et al., 2017).
Las vacunas vectoriales rHVT no sólo inducen una respuesta humoral, sino también una respuesta sistémica celular. La replicación de HVT en linfocitos de modo altamente asociado a células, induce un rango muy amplio de mecanismos de la respuesta inmune celular sistémica
Diversos estudios han demostrado que la vacunación con rHVT inducen una respuesta inmune celular sistémica a partir de las 3 semanas de vida (Rauw et al., 2010). Se debe tener en cuenta que las vacunas vectoriales rHVT no suelen inducir una respuesta inmune local mediada por anticuerpos como lo suelen hacer vacunas vivas (Reddy et al., 1996; Rauw et al., 2010). Por lo tanto, en aquellas patologías en que esta inmunidad juega un rol importante, la respuesta inmune generada por una vacuna vectorial rHVT será parcial, lo cual permite que en algunos casos siga habiendo excreción vírica a pesar de observarse una protección clínica de las aves (Reddy et al., 1996).
Nueva generación de vacunas vectoriales HVT: protección frente a tres enfermedades
Una de las principales desventajas de estas vacunas vectoriales HVT simples es que no se pueden combinar entre ellas, ni con otros virus HVT, dado que la replicación de dos virus HVT en el mismo huésped podría afectar la protección desarrollada frente a los antígenos insertados. Al no poderse combinar entre ellas ni con otros virus HVT obliga a tener que decidir frente a qué patología vacunamos a través de la vacuna vectorial.
Debido a la elección de frente a qué patología vacunamos el desarrollo de nuevas vacunas puede contener insertos frente a diferentes antígenos heterólogos era de mucha importancia
La inserción de más de un gen no es sencilla desde el punto de vista tecnológico, ya que aumenta la inestabilidad genética de la construcción. Hasta el momento, existían algunas vacunas rHVT a las que se habían insertado dos genes pero procedentes del mismo, pero hace un par de años, se describieron las primeras construcciones dobles rHVT ND-ILT (Morsey et al., 2015) y rHVT ND-IBD (Koopman, 2017). Tras su construcción, los primeros estudios in vitro demostraron la estabilidad genética y de expresión de los genes heterólogos insertados y se realizaron todos los tests in vivo para demostrar su seguridad en animales. Los estudios de protección demostraron que estas nuevas construcciones dobles generan protección frente a 3 enfermedades. Al vacunar al día de vida subcutáneo con una vectorial rHVT ND-IBD se genera protección frente a Gumboro a las 3 semanas, frente a ND a las 4 semanas y frente a Marek a partir de los 9 días. Dicha protección se ha demostrado como mínimo hasta las 8 semanas en IBD y ND y para todo el periodo de riesgo en caso de MD (Figura 3).