SALMONELLA INFANTIS, UNA PREOCUPACIÓN GLOBAL
Salmonella ha sido y sigue siendo un importante agente zoonótico transmitido por los alimentos, aunque es cierto que la prevalencia de infecciones en humanos ha disminuido significativamente en todo el mundo durante la última década.
SALMONELLA INFANTIS, UNA PREOCUPACIÓN GLOBAL
El aumento global de Salmonella Infantis ha causado preocupación, ya que poblaciones clonales altamente resistentes a los antimicrobianos y portadoras de factores de virulencia codificados por plásmidos se han identificado a nivel global en poblaciones de pollos (Alba et al., 2020; Guerrero et al., 2022).

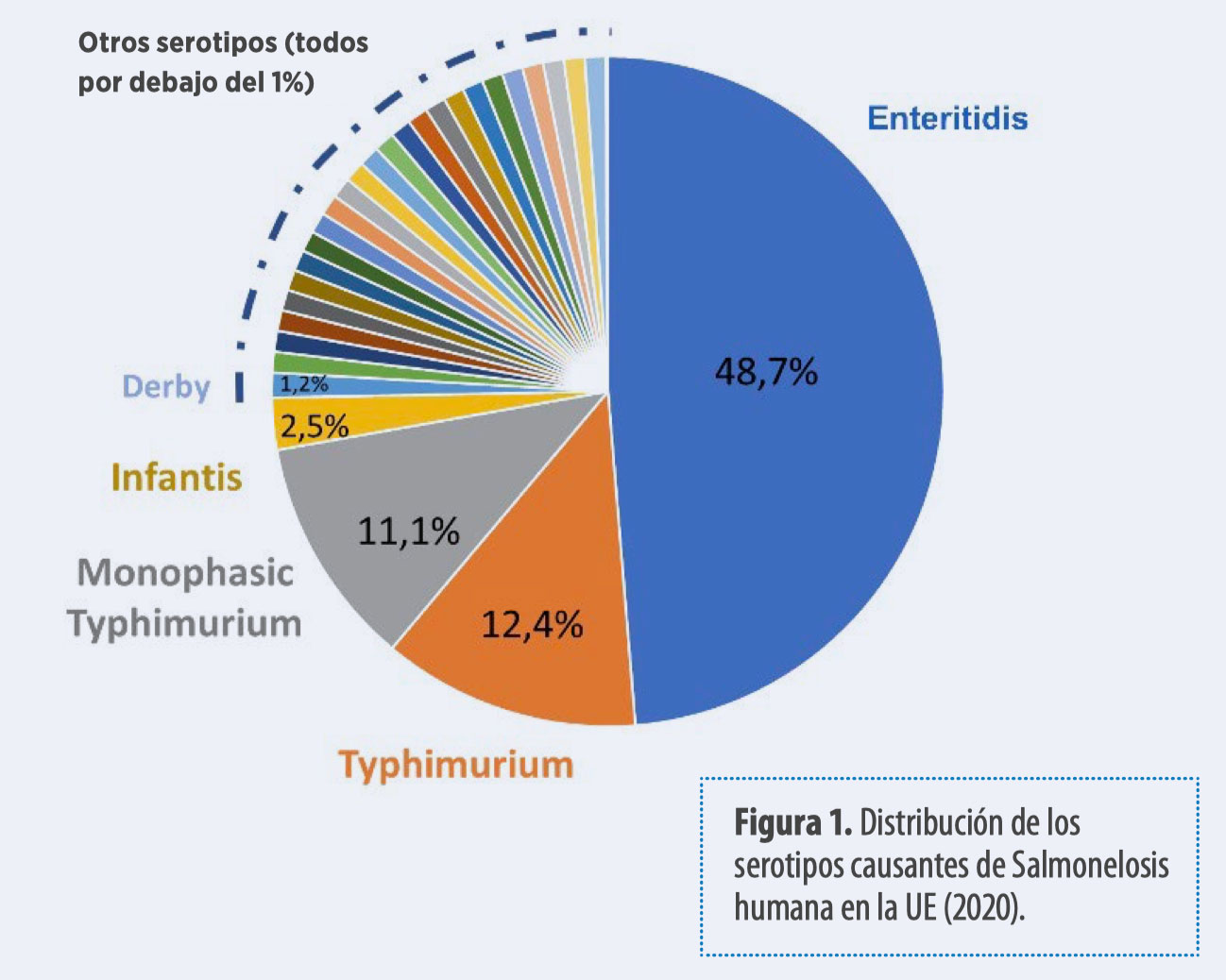
Este ha sido el principal serotipo aislado en la carne y granjas de pollos, aproximadamente representa el 50% de todos los aislamientos (EFSA, 2022).

Aunque esto todavía no ha provocado un fuerte aumento de los casos de intoxicación alimentaria humana, Salmonella Infantis se ha convertido en el tercer serotipo causante de intoxicación alimentaria humana (EFSA, 2022).
Además, a menudo se encuentra en la carne de pollo en los mataderos, lo que tiene implicaciones ya que la carne fresca de pollo debe estar libre de Salmonella.
|
El plásmido que está presente en los nuevos clones emergentes también se ha transferido a otros serotipos, según informes recientes, lo que hace que el problema sea potencialmente mayor de lo previsto inicialmente (Dos Santos et al., 2022).
Si bien los nuevos clones emergentes de Salmonella Infantis (y otros, por ejemplo, Paratyphi B, Heidelberg) persisten en gran medida en las granjas de pollos y, por lo tanto, la contaminación ambiental y la propagación horizontal son importantes, también las ponedoras y las reproductoras pueden ser colonizadas.
LA PROTECCIÓN ES FUNDAMENTAL PARA REDUCIR LA PREVALENCIA
Si bien la bioseguridad y el manejo son clave para el control de la infección en las granjas (y en los mataderos), la protección de ponedoras y reproductoras también puede contribuir a la reducción de la prevalencia de Salmonella Infantis.
Las vacunas utilizadas actualmente se basan principalmente en antígenos o cepas vivas de Salmonella Enteritidis o Typhimurium, ya que estos han sido los principales serotipos que contribuyen a las infecciones humanas.
Una de las principales dudas que ha surgido es si también se puede inducir la protección cruzada frente a otros serotipos de importancia mundial.
Salmonella se clasifica en serogrupos según la presencia de antígenos lipopolisacáridos (LPS) y, además, en serotipos según los antígenos LPS y flagelina.
Se describen más de 2000 serotipos y, aunque la mayoría puede causar infecciones en humanos, solo una docena se aísla con frecuencia de casos y brotes en humanos.
Siempre se ha creído que las cepas vacunales del mismo serotipo (o serogrupo) confieren una mejor protección contra las cepas del mismo serotipo (o serogrupo).

Inicialmente, en base a estudios de vacunas entre serotipos, muestran que las vacunas contra Salmonella Enteritidis y Gallinarum confieren protección cruzada entre sí.
Además, varios estudios muestran protección entre serogrupos, usando preparaciones de vacunas de un solo serotipo o vacunas que usan cepas de múltiples serotipos en una sola vacuna viva.
¿QUÉ SABEMOS SOBRE LOS EFECTOS DE LA PROTECCIÓN CRUZADA?
Los ejemplos de estudios sobre protección cruzada son numerosos.
Por ejemplo, Lee (2015) observó que después de la vacunación oral a ponedoras, con una cepa atenuada de Salmonella Typhimurium a los 7 días de edad seguida de una dosis de refuerzo a las 4 semanas, se originó una respuesta de anticuerpos significativa a los antígenos contra los serotipos Typhimurium, Gallinarum y Enteritidis.
Del mismo modo, se presenciaron respuestas linfoproliferativas significativas a los 3 serovares de Salmonella.
En este estudio, tras el desafío de Salmonella Gallinarum, el grupo inmunizado mostró:


También, se ha demostrado que la administración oral de una vacuna viva bivalente de Salmonella Enteritidis/Typhimurium causa una reducción de la colonización cecal por Salmonella Enteritidis y Infantis, esta última a niveles muy bajos, que estaban cerca del límite de detección (Eeckhaut et al., 2018).
En este estudio la vacuna viva bivalente de Salmonella Enteritidis/ Typhimurium fue administrada a las aves dos veces (el día 1 y la semana 6) y tres veces (el día 1, la semana 6 y 16). La infección fue en la semana 7 y 17, respectivamente.
Ambos estudios evidenciaron un nivel medio de colonización cecal por Salmonella de aproximadamente 10⁵ ufc/g en aves no vacunadas, mientras que la vacunación lo redujo a niveles que solo podían detectarse después de usarse cultivos de enriquecimiento.
Este estudio muestra una clara protección cruzada entre las vacunas con Enteritidis y Typhimurium y otros serotipos, en este caso Salmonella Infantis, un serotipo de un serogrupo diferente en comparación con Enteritidis y Typhimurium.
A pesar de que son necesarios estudios que lo confirmen, se espera que cuando se añaden múltiples serotipos a una preparación vacunal se puede inducir una protección cruzada más fuerte, ya que podrían estar presentes más antígenos.
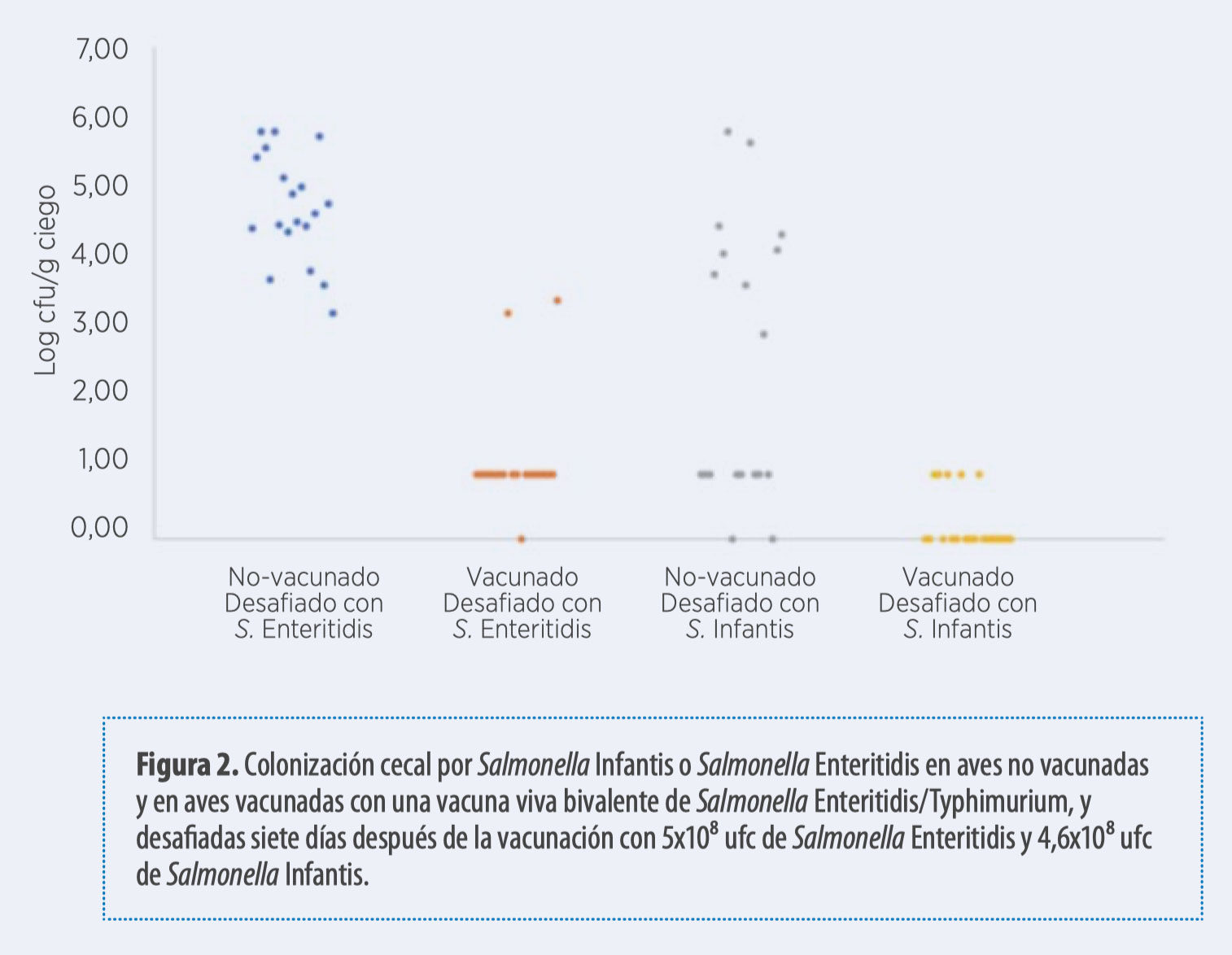
En conclusión, las vacunas contra Salmonella no solo pueden proporcionar protección entre serotipos, sino que también pueden conferir protección contra otros serotipos.
Todavía no se ha investigado si este es el caso para cualquier serotipo. Por lo tanto, es necesario realizar más estudios para respaldar esta afirmación, pero dado que muchos antígenos compartidos están presentes en las cepas de todos los serotipos de Salmonella, es de esperar la existencia de protección cruzada.
REFERENCIAS
Alba P, Leekitcharoenphon P, Carfora V, Amoruso R, Cordaro G, Di Matteo P, Ianzano A, Iurescia M, Diaconu EL, Study Group EN, Pedersen SK, Guerra B, Hendriksen RS, Franco A, Battisti A. (2020). Molecular epidemiology of Salmonella Infantis in Europe: insights into the success of the bacterial host and its parasitic pESI-like megaplasmid. Microb Genom. 6(5):e000365. doi: 10.1099/mgen.0.000365.
Calero-Cáceres W, Villacís J, Ishida M, Burnett E, Vinueza-Burgos C. (2020). Whole-Genome Sequencing of Salmonella enterica Serovar Infantis and Kentucky Isolates Obtained from Layer Poultry Farms in Ecuador. Microbiol Resour Announc. 26;9(13):e00091-20. doi: 10.1128/ MRA.00091-20.
Dos Santos AMP, Panzenhagen P, Ferrari RG, Conte-Junior CA. (2022). Large-scale genomic analysis reveals the pESI-like megaplasmid presence in Salmonella Agona, Muenchen, Schwarzengrund, and Senftenberg. Food Microbiol. 108:104112. doi: 10.1016/j.fm.2022.104112.
Eeckhaut V, Haesebrouck F, Ducatelle R, Van Immerseel F (2018). Oral vaccination with a live Salmonella Enteritidis/Typhimurium bivalent vaccine in layers induces cross-protection against caecal and internal organ colonization by a Salmonella Infantis strain. Vet. Microbiol. 218:7-12. doi: 10.1016/j.vetmic.2018.03.022.
EFSA. The European Union One Health (2021). Zoonoses Report. EFSA Journal, 20 (12), e07666. (https://efsa.onlinelibrary.wiley.com/doi/ abs/10.2903/j.efsa.2022.7666)
Guerrero T, Bayas-Rea R, Erazo E, Zapata Mena S (2020). Nontyphoidal Salmonella in Food from Latin America: A Systematic Review. Foodborne Pathog Dis. 19(2):85-103. doi: 10.1089/fpd.2020.2925.
Lapuz RR, Umali DV, Suzuki T, Shirota K, Katoh H (2012). Comparison of the prevalence of Salmonella infection in layer hens from commercial layer farms with high and low rodent densities. Avian Dis., 56(1):29-34. doi: 10.1637/9704-030711-Reg.1.
Lee, JH. (2015). Protection against salmonella typhimurium, salmonella gallinarum, and salmonella enteritidis infection in layer chickens conferred by a live attenuated salmonella typhimurium strain. Immune Netw. 15(1):27-36. doi: 10.4110/in.2015.15.1.27.


Materias Primas
Suscribete ahora a la revista técnica de avicultura
AUTORES

Temporización de los paneles de enfriamiento evaporativo
Michael Czarick
Infección por estafilococo en la población de reproductoras
Dra. Carolyn L. Miller Eric L. Jensen José J. Bruzual
Empresas conscientes: estrategias gerenciales para aumentar la productividad, mejorando el bienestar del personal que labora en la prefaena y el procesamiento
Eduardo Cervantes López
Alerta en seguridad alimentaria: la presencia de cloratos
Jose Luis Valls
Gases efecto invernadero y ganadería: ciencia frente a titulares alarmistas
Juan Pascual-VP Elanco
Bacterias en la planta de incubación: impacto y estrategias de control
Renata Steffen
Gestión de los riesgos asociados a Histomonas y coccidios mediante plantas y sustancias aromáticas
A. A. Mahieu A. Canin A. Greuter D. Liebhart F. Laurent J-M Watier M. Aoun M. Hess R. Domitile
Alphitobius diaperinus: un problema en la avicultura
Alice Silva
El huevo como alimento funcional y sus componentes
Pedro Gil Sevillano
La importancia real de los niveles de las unidades formadoras de placas (UFP) en las vacunas de marek
Isabel M Gimeno -DVM PhD
Alimentación de ponedoras de larga vida productiva
Ing. Agr. Msc Manuel Vázquez - Nutricionista
Salud digestiva en avicultura: Estrategias integrales y el rol de BILANTUL solución para optimizar el rendimiento productivo
Laura Rodríguez
2027 Está a la vuelta de la esquina, di adiós a las jaulas